题目内容
【题目】实验室有甲乙两瓶久 置的氢氧化钠固体,某学 习小组为了研究其变质情 况,进行了如下实验:(电子秤示数单位为克)
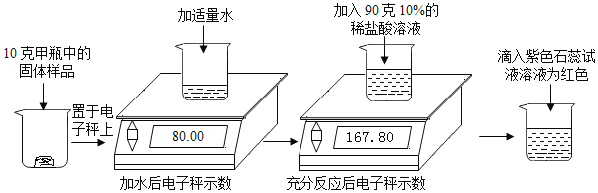
(1)滴入紫色石蕊试液后 溶液为红色,说明反应后溶液呈_____性。
(2)上述实验中产生的二氧化碳气体质量为_____克。
(3)计算甲瓶固体样品中碳酸钠的质量分数_____。
【答案】酸 2.20 甲瓶固体样品中碳酸钠的质量分数53%
【解析】
(1)滴入紫色石蕊试液后溶液为红色,说明反应后溶液呈酸性。
(2)根据质量守恒定律,产生的二氧化碳气体质量为:80.00g+90g﹣167.80g=2.20g;
(3)设固体样品中碳酸钠的质量为x
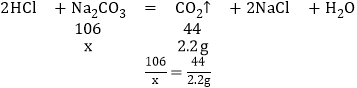
解得:x=5.30g
固体样品中碳酸钠的质量分数![]() ×100%=53%。
×100%=53%。
故答案为:(1)酸;(2)2.20; (3)甲瓶固体样品中碳酸钠的质量分数53%。

【题目】“卓筒井”是手工制盐的活化石,是我国古代劳动人民勤劳、智慧的象征。其工艺流程包括下面五个步骤:钻井→汲卤→晒卤→滤卤→煎盐。请回答下列问题:
(1)上述步骤中,_____与实验室过滤的原理一样,“煎盐”和实验室_____结晶的原理相同。
(2)“汲卤”获得卤水主要成分是氯化钠与氯化钾,卤水中氯化钠的质量分数大约为 7%~10%,“晒卤”目的是_____;“煎盐”得到的食盐中含有氯化钾,实验室可用_____检验,操作方法是_____。
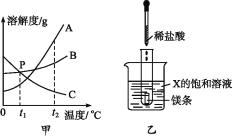
(3)下列数据是氯化钠和氯化钾固体在不同温度时的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 g/100g 水 | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 | |
根据表中数据可得出:40℃时,氯化钠溶解度_____氯化钾溶解度(填:大于、小于、等于); 氯化钠与氯化钾溶解度相同的温度范围是_____;20℃时,100g 卤水氯化钠的质量分数为 9%,含氯化钾 1.00g,蒸发掉水大于_____g,开始有氯化钠析出。
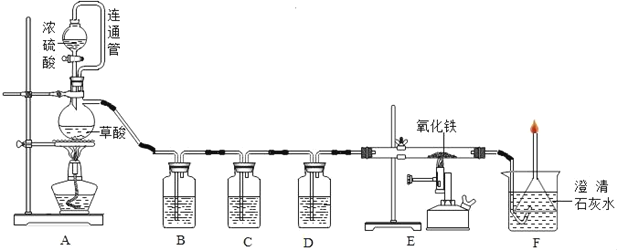
【题目】某化工厂用废硫酸制备K2SO4的流程如下:
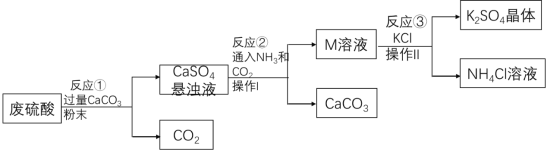
(l)生产上将CaCO3研成粉末的目的是_____;写出反应①的化学方程式:_____,操作I的名称是_____。
(2)上述流程中,除可综合利用CO2外,还可循环使用的物质是_____(写化学式)。
(3)写出反应③的化学方程式:_____,反应③在常温下能实现的原因是_____。(反应③中相关物质的溶解度见下表)
物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
(4)洗涤反应③所得晶体不用水而用饱和K2SO4溶液的目的是_____。