题目内容
实验室对二氧化碳的制取和性质的探究
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
从制取和收集的角度分析,一般选择第①组药品,该组药品发生反应的文字表达式为
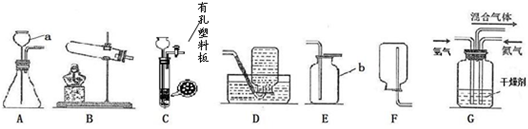
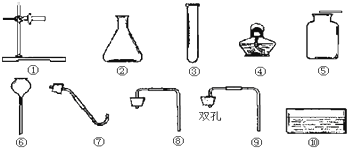
(2)选择装置.通过对制取氧气装置的分析,他选择用过氧化氢制取氧气的发生装置.你认为他选择的依据是
(3)制取气体.将药品装入所选装置制取气体,并用
(4)气体检验.将燃着的木条伸入气体中,木条立即熄灭,因此他确定该气体是二氧化碳.他的检验方法是否正确?请说明理由.
(5)如图所示,请回忆老师做的“倾倒二氧化碳”的演示实验,回答问题: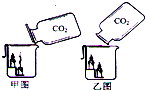
甲、乙两同学共同收集满两瓶质量相同的二氧化碳气体,并分别将二氧化碳气体慢慢倒入烧杯中,请分析回答:
①甲同学用甲图的倾倒方式向烧杯中倾倒足够的二氧化碳,我们观察到两根蜡烛是由下而上熄灭,请你告诉我们,为什么是由下而上熄灭?
②乙同学用乙图的倾倒方式向烧杯中倾倒足够的二氧化碳,我们观察到的结果是两根蜡烛都没有熄灭,请你联系知识分析,用乙图的倾倒方式为什么二氧化碳没有进入烧杯?
(6)如图所示,请回忆教材中“酒精灯的使用方法”,回答问题: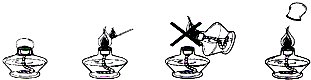
①只能用燃着的火柴或细木条去点燃酒精灯,用酒精灯引燃另一只酒精灯会引起失火,原因是
②为避免引起失火,用完酒精灯后,不能立即向酒精灯里添加酒精,应该用灯帽盖灭并且使酒精灯
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率非常快 |
碳酸钙+盐酸→氯化钙+二氧化碳+水
碳酸钙+盐酸→氯化钙+二氧化碳+水
;不选择第③组药品的原因是反应太快来不及收集
反应太快来不及收集
如果要解决这个问题可将长颈漏斗改为分液漏斗或针筒
分液漏斗或针筒
(一种实验仪器).(2)选择装置.通过对制取氧气装置的分析,他选择用过氧化氢制取氧气的发生装置.你认为他选择的依据是
药品状态或固体和液体反应
药品状态或固体和液体反应
和反应条件或不要加热或常温
反应条件或不要加热或常温
.(3)制取气体.将药品装入所选装置制取气体,并用
向上排空气
向上排空气
法收集.验满方法是用燃着的木条伸到集气瓶口,若立即熄灭,则已满
用燃着的木条伸到集气瓶口,若立即熄灭,则已满
.(4)气体检验.将燃着的木条伸入气体中,木条立即熄灭,因此他确定该气体是二氧化碳.他的检验方法是否正确?请说明理由.
不正确,因为不能支持燃烧的气体不是只有二氧化碳一种
不正确,因为不能支持燃烧的气体不是只有二氧化碳一种
.正确检验二氧化碳的方法所发生反应的文字表达式是二氧化碳+氢氧化钙→碳酸钙+水
二氧化碳+氢氧化钙→碳酸钙+水
.(5)如图所示,请回忆老师做的“倾倒二氧化碳”的演示实验,回答问题:

甲、乙两同学共同收集满两瓶质量相同的二氧化碳气体,并分别将二氧化碳气体慢慢倒入烧杯中,请分析回答:
①甲同学用甲图的倾倒方式向烧杯中倾倒足够的二氧化碳,我们观察到两根蜡烛是由下而上熄灭,请你告诉我们,为什么是由下而上熄灭?
由于CO2密度比空气大,沿烧杯壁流到底部,下面的蜡烛首先接触到CO2,由于CO2不燃烧也不支持燃烧,故由下向上逐渐熄灭
由于CO2密度比空气大,沿烧杯壁流到底部,下面的蜡烛首先接触到CO2,由于CO2不燃烧也不支持燃烧,故由下向上逐渐熄灭
.②乙同学用乙图的倾倒方式向烧杯中倾倒足够的二氧化碳,我们观察到的结果是两根蜡烛都没有熄灭,请你联系知识分析,用乙图的倾倒方式为什么二氧化碳没有进入烧杯?
乙图的倾倒方式,没用玻璃片掩盖,直接倒在火焰的上方,由于蜡烛燃烧放热,使得气体受热,密度变小,故CO2不能与蜡烛火焰接触而跑到空气去了
乙图的倾倒方式,没用玻璃片掩盖,直接倒在火焰的上方,由于蜡烛燃烧放热,使得气体受热,密度变小,故CO2不能与蜡烛火焰接触而跑到空气去了
.(6)如图所示,请回忆教材中“酒精灯的使用方法”,回答问题:

①只能用燃着的火柴或细木条去点燃酒精灯,用酒精灯引燃另一只酒精灯会引起失火,原因是
用酒精灯去引燃另一只酒精灯时,酒精灯倾斜可能会流出酒精,故会引起失火
用酒精灯去引燃另一只酒精灯时,酒精灯倾斜可能会流出酒精,故会引起失火
.②为避免引起失火,用完酒精灯后,不能立即向酒精灯里添加酒精,应该用灯帽盖灭并且使酒精灯
冷却
冷却
后,再添加酒精.分析:(一)对比实验的设计方法是只能允许有一种变量,对照实验①②只有加入的酸不同;对照实验①③只有石灰石的形状不同;不选择第②组药品的原因是碳酸钙与硫酸反应,生成硫酸钙微溶于水,覆盖在石灰石表面,里面的石灰石不能与硫酸接触,使反应速度减慢并停止;碳酸钠是白色粉末,与稀盐酸反应时速度太快,不利于收集二氧化碳气体.
(二)二氧化碳有三个化学性质:既不能燃烧也不能支持燃烧,还不能供给呼吸;能与水反应;能与石灰水反应(即能与碱溶液反应).学会二氧化碳的验满方法和检验方法.将燃着的木条放在集气瓶口,观察火焰是否熄灭;要用石灰水检验.记牢酒精灯的使用方法和注意事项.
(二)二氧化碳有三个化学性质:既不能燃烧也不能支持燃烧,还不能供给呼吸;能与水反应;能与石灰水反应(即能与碱溶液反应).学会二氧化碳的验满方法和检验方法.将燃着的木条放在集气瓶口,观察火焰是否熄灭;要用石灰水检验.记牢酒精灯的使用方法和注意事项.
解答:解:(1)碳酸钙和盐酸生成氯化钙和二氧化碳和水,碳酸钠是白色粉末,与稀盐酸反应时速度太快,不利于收集二氧化碳气体.如果要改进,可以改用分液漏斗或针筒,控制加药品的速度.故答案为:碳酸钙+盐酸→氯化钙+二氧化碳+水;反应太快来不及收集;分液漏斗或针筒
(2)选择用过氧化氢制取氧气的发生装置的依据是:药品状态或固体和液体反应、反应条件或不要加热或常温.故答案为:药品状态或固体和液体反应、反应条件或不要加热或常温
(3)由于CO2密度比空气大,能溶于水,因此只能用向上排空气法收集;验满方法是:将燃着的木条放在集气瓶口,观察火焰是否熄灭.故答案为:向上排空气法;用燃着的木条伸到集气瓶口,若立即熄灭,则已满.
(4)二氧化碳和氮气都既不能燃烧也不能支持燃烧,二氧化碳要用石灰水检验.故答案为:不正确,因为不能支持燃烧的气体不是只有二氧化碳一种;二氧化碳+氢氧化钙→碳酸钙+水、
(5)此实验证明了二氧化碳的一个物理性质和一个化学性质,但是要注意热的气流向上走.故答案为:①由于CO2密度比空气大,沿烧杯壁流到底部,下面的蜡烛首先接触到CO2,由于CO2不燃烧也不支持燃烧,故由下向上逐渐熄灭;②乙图的倾倒方式,没用玻璃片掩盖,直接倒在火焰的上方,由于蜡烛燃烧放热,使得气体受热,密度变小,故CO2不能与蜡烛火焰接触而跑到空气去了.
(6)点燃酒精灯用火柴,熄灭酒精灯用灯帽盖灭,绝对禁止用一个酒精灯去引燃另一只酒精灯时,会引起失火.故答案为:①用酒精灯去引燃另一只酒精灯时,酒精灯倾斜可能会流出酒精,故会引起失火.②冷却.
(2)选择用过氧化氢制取氧气的发生装置的依据是:药品状态或固体和液体反应、反应条件或不要加热或常温.故答案为:药品状态或固体和液体反应、反应条件或不要加热或常温
(3)由于CO2密度比空气大,能溶于水,因此只能用向上排空气法收集;验满方法是:将燃着的木条放在集气瓶口,观察火焰是否熄灭.故答案为:向上排空气法;用燃着的木条伸到集气瓶口,若立即熄灭,则已满.
(4)二氧化碳和氮气都既不能燃烧也不能支持燃烧,二氧化碳要用石灰水检验.故答案为:不正确,因为不能支持燃烧的气体不是只有二氧化碳一种;二氧化碳+氢氧化钙→碳酸钙+水、
(5)此实验证明了二氧化碳的一个物理性质和一个化学性质,但是要注意热的气流向上走.故答案为:①由于CO2密度比空气大,沿烧杯壁流到底部,下面的蜡烛首先接触到CO2,由于CO2不燃烧也不支持燃烧,故由下向上逐渐熄灭;②乙图的倾倒方式,没用玻璃片掩盖,直接倒在火焰的上方,由于蜡烛燃烧放热,使得气体受热,密度变小,故CO2不能与蜡烛火焰接触而跑到空气去了.
(6)点燃酒精灯用火柴,熄灭酒精灯用灯帽盖灭,绝对禁止用一个酒精灯去引燃另一只酒精灯时,会引起失火.故答案为:①用酒精灯去引燃另一只酒精灯时,酒精灯倾斜可能会流出酒精,故会引起失火.②冷却.
点评:熟练记忆:二氧化碳的实验室制法:固+液,不需加热;反应原理、发生装置和收集装置用到的仪器,以及其检验和验满的方法和操作;还有酒精灯的使用方法等;学会用探究的方法研究实验问题.气体的制取装置的选择与反应物的状态和反应的条件有关;药品的选择也与药品的状态和性质有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
星期天,小青发现妈妈正在炸制一种面食,当将做好的一小块面饼放入热的油锅中,面饼迅速膨胀,他对此颇感兴趣,决定对其进行探究.妈妈告诉他调面时使用了发酵粉.小青想起在化学课中学过发酵粉的主要成分碳酸氢钠(NaHCO3),他决定将一包发酵粉带到学校实验室与同学一起进行探究.
Ⅰ.发酵粉溶液酸碱性如何?(请你完成下列表格中的空白)
Ⅱ.小青认为面饼膨胀是由于炸制过程中,产生了大量的二氧化碳气体所致,他对二氧化碳的来源作了两种猜测:
猜测 ①:二氧化碳可能是由碳酸氢钠与面团中的酸性物质反应产生的;
猜测 ②:二氧化碳可能是由碳酸氢钠受热分解产生的.
针对以上猜测,小青设计了以下实验:(请你完成下列表格中的空白)
实验2碳酸氢钠受热分解的化学方程式 ;
Ⅲ.应用:在蒸馒头时,我们通常在发酵后的面团中加入小苏打(NaHCO3),加入NaHCO3的目的是 .
Ⅰ.发酵粉溶液酸碱性如何?(请你完成下列表格中的空白)
| 实验步骤 | 实验现象 | 实验结论 |
| 发酵粉的溶液显碱性 |
猜测 ①:二氧化碳可能是由碳酸氢钠与面团中的酸性物质反应产生的;
猜测 ②:二氧化碳可能是由碳酸氢钠受热分解产生的.
针对以上猜测,小青设计了以下实验:(请你完成下列表格中的空白)
| 实验步骤 | 实验现象 | 实验 结论 | |
| 实验1 | 猜想①正确 | ||
| 实验2 | 猜想②正确 |
Ⅲ.应用:在蒸馒头时,我们通常在发酵后的面团中加入小苏打(NaHCO3),加入NaHCO3的目的是