题目内容
【题目】纯碱用途广泛。工业上可用废碱渣(主要成分 Na2CO3)吸收硫酸厂尾气中的 SO2 制备无水Na2SO3,达到减少污染、节约资源的目的。反应过程中溶液组成变化如图所示。 下列说法正确的是( )
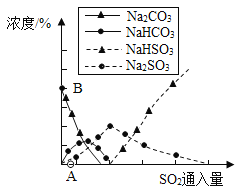
A.吸收初期(图中 A 点以前)反应的化学方程式为:SO2+H2O+2Na2CO3= Na2SO3+2NaHCO3
B.不断通入 SO2 最终产物是:Na2SO3 和 NaHSO3
C.纯碱属于碱,其溶液显碱性
D.溶液中可能同时存在 Na2CO3 和 NaHSO3
【答案】A
【解析】
A、由图可知,吸收初期,碳酸钠质量逐渐减小,碳酸氢钠和亚硫酸钠质量逐渐增加,故是碳酸钠、二氧化硫和水反应生成碳酸氢钠和亚硫酸钠,反应的化学方程式为2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3,故正确;
B、由图可知,不断通入SO2,最终产物是亚硫酸氢钠,故错误;
C、纯碱是碳酸钠,是由金属离子和酸根离子组成的化合物,属于盐,故错误;
D、据图可知,Na2CO3 和 NaHSO3不能同时存在,故错误。
故选A。

练习册系列答案
相关题目