题目内容
【题目】合成氨是人类科学技术上的一项重大突破,对社会发展与科技进步做出了巨大贡献。合成氨工艺的主要流程如下:
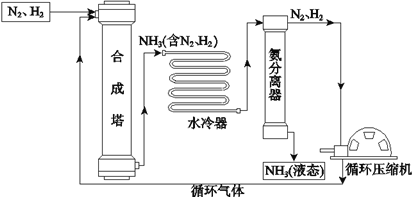
(1)合成塔中的反应在高温、高压、催化剂条件下进行,其化学方程式是____________。
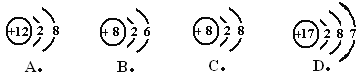
(2)上述反应中,一定发生改变的是_____(填字母序号)。
A.元素种类 B. 分子种类 C. 原子种类
(3)生产过程中可循环使用的物质是_____。
(4)根据表中的数据回答问题。
物质 | H2 | N2 | NH3 |
沸点/℃(1.01×105 Pa) | –252 | –195.8 | –33.35 |
在1.01×105 Pa时,要将工业合成氨的产物氨气(NH3)从它的反应物氮气和氢气的混合物中分离开来,最适宜的温度应该控制在________℃≤ T <________℃。
【答案】 N2+3H2 ![]() 2NH3 B N2、H2 -195.8℃ -33.35℃
2NH3 B N2、H2 -195.8℃ -33.35℃
【解析】(1)合成塔中的反应在高温、高压、催化剂条件下进行,其化学方程式是N2+3H2 ![]() 2NH3 。 (2)上述反应中,一定发生改变的是B. 分子种类,化学变化的实质是分子的划分,原子的重新组合。(3)生产过程中可循环使用的物质是N2、H2 。(4)根据表中的数据回答问题。要将工业合成氨的产物氨气(NH3)从它的反应物氮气和氢气的混合物中分离开来,最适宜的温度应该控制在-195.8℃ ≤ T <-33.35℃,利用液体物质沸点不同分离。
2NH3 。 (2)上述反应中,一定发生改变的是B. 分子种类,化学变化的实质是分子的划分,原子的重新组合。(3)生产过程中可循环使用的物质是N2、H2 。(4)根据表中的数据回答问题。要将工业合成氨的产物氨气(NH3)从它的反应物氮气和氢气的混合物中分离开来,最适宜的温度应该控制在-195.8℃ ≤ T <-33.35℃,利用液体物质沸点不同分离。
点睛∶化学变化的实质是分子的划分,原子的重新组合,分子种类一定会变化,原子种类和数量一定不会变化。

 阅读快车系列答案
阅读快车系列答案【题目】溶解度可表示物质溶解性的大小。
①左下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
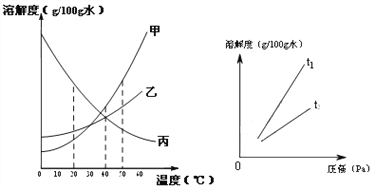
Ⅰ.20℃时,甲的溶解度________(填“>”、“<”或“=”)乙的溶解度。
Ⅱ.40℃时,乙和丙________(填“能”或“不能”)形成溶质质量分数相同的饱和溶液。
Ⅲ.20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃。请填写下表。
烧杯中的溶质 | 烧杯中固体的变化 |
甲 | __________________ |
乙 | 固体逐渐减少至全部溶解 |
丙 | __________________ |
②气体的溶解度也有一定的变化规律。
Ⅰ.打开可乐瓶,逸出大量气泡。由此可见,压强越小,CO2的溶解度越_________。为增大CO2的溶解度,可采用的一种方法是________。
Ⅱ.不同温度下,氧气的溶解度随压强的变化如右图所示,图中t1对应的温度为40℃,则t2对应的温度________(填编号)。
a.大于40℃ b.小于40℃ c.无法确定