题目内容
质量分数和质量都相同的三份稀盐酸,分别与镁、铝和锌三种金属恰好完全反应,并得到无色澄清溶液,同时收集到质量分别为以a、b、c的氢气,则所收集到的氢气质量的大小关系是( )A.a=c>b
B.a>b>c
C.c>b>a
D.a=b=c
【答案】分析:金属与酸反应生成的氢气全部来源于盐酸中所含的氢元素,根据题意:质量分数和质量都相同的三份稀盐酸,分别与镁、铝和锌三种金属恰好完全反应,三种金属消耗盐酸的质量相等,则得到相同质量的氢气.
解答:解:反应生成的氢气来源于盐酸中所含的氢元素,质量分数和质量都相同的三份稀盐酸,分别与镁、铝和锌三种金属恰好完全反应,说明三种金属消耗盐酸的质量相等,盐酸所含的氢元素相等,则得到相同质量的氢气;
故选D.
点评:明确金属与酸反应的原理,并了解化学反应前后元素的质量、种类守恒,仔细分析题意即可顺利解答.
解答:解:反应生成的氢气来源于盐酸中所含的氢元素,质量分数和质量都相同的三份稀盐酸,分别与镁、铝和锌三种金属恰好完全反应,说明三种金属消耗盐酸的质量相等,盐酸所含的氢元素相等,则得到相同质量的氢气;
故选D.
点评:明确金属与酸反应的原理,并了解化学反应前后元素的质量、种类守恒,仔细分析题意即可顺利解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
Fe、Mg、Al三种金属分别跟稀盐酸充分反应,得到相同质量的氢气,其原因是( )
| A、Fe,Mg、Al的质量相等,盐酸足量 | B、Fe,Mg、Al的质量比是28:12:9,盐酸足量 | C、Fe,Mg、A1的质量比是56:24:27,盐酸足量 | D、Fe,Mg、Al均为过量,所用盐酸的质量分数和质量都相同 |
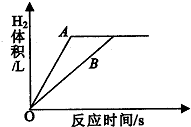 积(气体体积都在相同状况下测定)与反应时间的关系如下图所示.根据此图请你写出两条结论.
积(气体体积都在相同状况下测定)与反应时间的关系如下图所示.根据此图请你写出两条结论.