题目内容
【题目】工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质),精制的工艺流程如下:
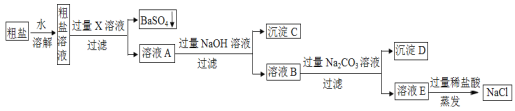
(1)X中含有的阳离子是________________;沉淀C的化学式是_____________。
(2)写出生成沉淀D的一个化学方程式_______________________________________。
(3)溶液E中加过量稀盐酸的作用是________________________________________。
【答案】Ba2+ Mg(OH)2 CaCl2+Na2CO3=CaCO3↓+2NaCl或BaCl2+Na2CO3=BaCO3↓+2NaCl 除尽过量的Na2CO3
【解析】
工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质)的精制实际上是除去镁离子、钙离子、硫酸根离子的过程。
(1)粗盐中含有MgCl2、CaCl2、Na2SO4等杂质,所以X中含有的阳离子是Ba2+,X是氯化钡溶液,加入过量的X生成了硫酸钡沉淀;溶液A中含有镁离子,氢氧根离子和镁离子会生成氢氧化镁沉淀,所以沉淀C的化学式是Mg(OH)2;
(2)碳酸根离子和钙离子、钡离子会生成碳酸钙沉淀、碳酸钡沉淀,所以生成沉淀D的化学方程式是:CaCl2+Na2CO3=CaCO3↓+2NaCl或BaCl2+Na2CO3=BaCO3↓+2NaCl;
(3)加入的过量的碳酸钠和氢氧化钠对于氯化钠也是杂质,所以溶液E中加过量稀盐酸的作用是:除尽过量的碳酸钠和氢氧化钠。

 名校课堂系列答案
名校课堂系列答案【题目】下列是电解水反应示意图和装置。示意图①~③中,“●”表示氢原子,“O”表示氧原子。
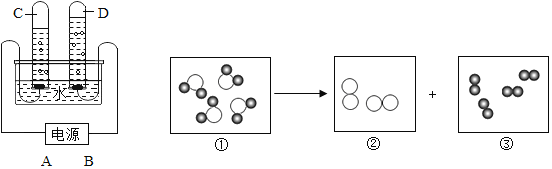
(1)图中表示化合物的是_____,表示单质的是_____(用序号填空)。
(2)②所代表的物质是左图中试管(填字母)_____中产生的气体,图中A是电源的_____(填“正”或“负”)极。
(3)为了探究C和D玻璃管分别产生的是什么气体,用燃着的木条分别在两个玻璃管口检验电解反应中产生的气体,观察并记录发生的现象,请填写下表:
C玻璃管 | D玻璃管 | |
现象 | _____ | _____ |
解释 | _____ | _____ |
(4)写出图中反应的化学符号表达式:_____。
【题目】如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y,若挤压胶头滴管使液体滴入广口瓶中,振荡,一段时间后可见小气球a膨胀鼓起。下表中的各组物质不会出现上述现象的是( )
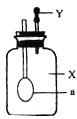
X | Y | |
A | CO | Ca(OH)2溶液 |
B | CO2 | NaOH溶液 |
C | HCl | Ca(OH)2溶液 |
D | SO2 | NaOH溶液 |
A. AB. BC. CD. D
【题目】学习了二氧化锰过氧化氢分解有催化作用的知识后,某兴趣小组的同学提出问题:氧化铁能否起到类似于二氧化锰的催化作用呢?于是他们进行了以下探究.
(猜想)
Ⅰ.氧化铁不是反应的催化剂、也不参与反应,质量和化学性质反应前后均不变;
Ⅱ.氧化铁参与反应产生氧气,反应前后质量不变,但化学性质发生了改变;
Ⅲ.氧化铁是反应的催化剂,反应前后_____.
(实验)用天平称0.2g氧化铁,用试管取5mL 5%的过氧化氢溶液,进行如下实验:
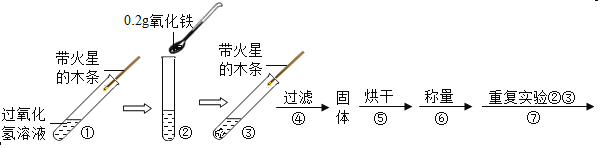
(注:氧化铁不溶于水,过滤可与水分离)
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
带火星的木条复燃. | _____ | 过氧化氢溶液中:_____ | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
(2)步骤①的目的是_____.
(3)写出上述有关过氧化氢分解的文字表达式_____.
(4)步骤⑦重复实验②、③的目的是_____.
(继续探究)从上述实验得出氧化铁是反应的催化剂.对同种催化剂,有哪些因素可能影响催化效果?请提出猜想并设计实验进行探究._____(注意:至少探究两种因素,答对一种因素奖励2分,本題最多奖励4分,化学试卷总分不超过60分)