题目内容
被称为“绿色氧化剂”的过氧化氢(H2O2)俗称双氧水,是一种无色液体,常用作无公害的消毒剂和漂白剂等.在有少量催化剂的条件下,它迅速分解,生成水和氧气.某同学想探究二氧化锰是否能作过氧化氢分解的催化剂.请你设计实验的方法步骤,预测可能的实验结果等,来帮助他解决问题.
(1)方法步骤:
①在试管中加入5mL 15%的过氧化氢溶液,用________.
(2)预测可能出现的实验现象及相应的结论:
第一步现象及结论:________,
第二步的现象及结论:________.
(3)如果二氧化锰能作双氧水分解的催化剂.分离反应混合物中的MnO2,洗净、干燥、称量,其质量将________(填:增大、减小、不变);此反应化学方程式为________.
解:(1)氧气具有助燃性能使带火星的木条复燃.①在试管中加入5mL 15%的过氧化氢溶液,用带火星木条伸入试管内;②再加入少量二氧化锰后,用带火星木条伸入试管内;
(2)预测可能出现的实验现象及相应的结论:
第一步现象:木条没有复燃;结论:没有氧气生成;
第二步的现象木条复燃;结论:有氧气生成;
(3)如果二氧化锰能作双氧水分解的催化剂.分离反应混合物中的MnO2,洗净、干燥、称量,其质量将不变;反应化学方程式为2H2O2 2H2O+O2↑.
2H2O+O2↑.
故答案为:(1)用带火星木条伸入试管内;②再加入少量二氧化锰后,用带火星木条伸入试管内;
(2)现象:木条没有复燃;结论:没有氧气生成;
现象:木条复燃;结论:有氧气生成;
(3)不变;2H2O2 2H2O+O2↑.
2H2O+O2↑.
分析:根据氧气具有助燃性能使带火星的木条复燃以及催化剂改变其它反应的化学反应速率,本身的质量和化学性质在化学反应前后都不变进行解答.
点评:本题要抓住催化剂的特点“一变、二不变”.即改变其它反应的化学反应速率,本身的质量和化学性质在化学反应前后都不变,就可以设计有关的实验步骤.本考点主要出现在实验题中.
(2)预测可能出现的实验现象及相应的结论:
第一步现象:木条没有复燃;结论:没有氧气生成;
第二步的现象木条复燃;结论:有氧气生成;
(3)如果二氧化锰能作双氧水分解的催化剂.分离反应混合物中的MnO2,洗净、干燥、称量,其质量将不变;反应化学方程式为2H2O2
 2H2O+O2↑.
2H2O+O2↑.故答案为:(1)用带火星木条伸入试管内;②再加入少量二氧化锰后,用带火星木条伸入试管内;
(2)现象:木条没有复燃;结论:没有氧气生成;
现象:木条复燃;结论:有氧气生成;
(3)不变;2H2O2
 2H2O+O2↑.
2H2O+O2↑.分析:根据氧气具有助燃性能使带火星的木条复燃以及催化剂改变其它反应的化学反应速率,本身的质量和化学性质在化学反应前后都不变进行解答.
点评:本题要抓住催化剂的特点“一变、二不变”.即改变其它反应的化学反应速率,本身的质量和化学性质在化学反应前后都不变,就可以设计有关的实验步骤.本考点主要出现在实验题中.

练习册系列答案
相关题目
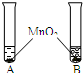
 ①将等体积的两种无色液体分别加入A、B两个试管中.
①将等体积的两种无色液体分别加入A、B两个试管中.