题目内容
【题目】根据下图所示,按要求回答问题:
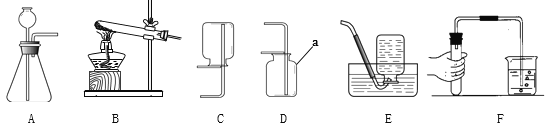
(1)写出图中仪器的名称:a ________, 图F实验的目的是__________。
(2)实验室用加热氯酸钾和二氧化锰混合物的方法制取并收集的氧气时,应选用的装置是______和 ______(填字母序号),该反应的文字(或符号)表达式为______。
(3)在题(2)的反应中质量和化学性质都没有改变的物质是________,若用D收集氧气,检验氧气已集满的方法是_______。
(4)若实验室用加热高锰酸钾的方法制取并用排水法收集氧气,实验时应在试管口放一团棉花,其作用是________。
【答案】集气瓶 检查装置气密性 B D或E 氯酸钾![]() 氯化钾+氧气(或KClO3
氯化钾+氧气(或KClO3![]() KCl+O2) 二氧化锰 将带火星的木条伸到集气瓶口处 防止高锰酸钾颗粒进入导管污染气体
KCl+O2) 二氧化锰 将带火星的木条伸到集气瓶口处 防止高锰酸钾颗粒进入导管污染气体
【解析】
(1)仪器a的名称是集气瓶,故填集气瓶;
图F实验的目的是检查装置的气密性,故填检查装置的气密性。
(2)实验室用加热氯酸钾和二氧化锰混合物制取仪器,是固体受热生成气体,发生装置性质固体受热发生装置,故选B;
氧气的密度大于空气的密度,且氧气不溶于水,所以收集氧气既能用向上排空气法,也可以用排水法,故选D或E;
氯酸钾在二氧化锰作催化剂的条件下反应生成氯化钾和氧气,故文字表达式写为:氯酸钾![]() 氯化钾+氧气,符号表达式写为:KClO3
氯化钾+氧气,符号表达式写为:KClO3![]() KCl+O2,故填氯酸钾
KCl+O2,故填氯酸钾![]() 氯化钾+氧气(或KClO3
氯化钾+氧气(或KClO3 ![]() KCl+O2)。
KCl+O2)。
(3)在题(2)的反应中质量和化学性质都没有改变的物质是催化剂,即二氧化锰,故填二氧化锰;
D为向上排空气法,向上排空气法收集氧气时验满的方法是将带火星的木条伸到集气瓶口处,观察木条是否复燃,故填将带火星的木条伸到集气瓶口处。
(4)用加热高锰酸钾的方法制取氧气,实验时应在试管口放一团棉花,其作用是防止高锰酸钾颗粒进入导管污染气体,故填防止高锰酸钾颗粒进入导管污染气体。

 阅读快车系列答案
阅读快车系列答案【题目】某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰。该小组同学进行了如下探究。
(1)探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由_________(填“固态”或“气态”)物质燃烧形成的。

(2)探究二:物质燃烧产生火焰的根本原因是什么?
(查阅资料)
物质 | 熔点/℃ | 沸点/℃ | 燃烧时温度/℃ |
石蜡 | 50~70 | 300~500 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由上表可知:物质燃烧能否产生火焰与其________(填“熔点”或“沸点”)和燃烧时温度有关。由此推测:钠在燃烧时,__________(填“有”或“没有”)火焰产生。
(3)根据硫在空气或氧气中燃烧的实验事实,请你推测硫沸点______硫燃烧时的温度(填“>”或“<”或“=”)
【题目】甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:
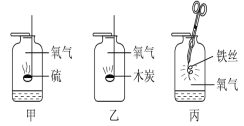
(1)所发生的三个反应有多个共同的特点,分别是:①________,②______。(写两点即可)
(2)甲、丙两实验集气瓶中均放少量水,甲中加入少量水的目的是___________,甲瓶中反应的文字表达式为__________。
(3)小明做完上述实验后,在乙中加入了一种无色液体,加该液体的目的是 _______。
(4)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。他将镁条和不同含碳量的铁丝(铁丝直径均为0.4 mm)放入氧气中燃烧,并将现象记录在下表中。
物质 | 镁 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 | 剧烈燃烧,火星四射 |
①小明实验前将铁丝绕成螺旋状的目的是___________。
②造成铁丝在氧气中燃烧时火星四射的主要原因是 ____________。
③铁丝在氧气中燃烧的文字表达式为 ___________。





