题目内容
【题目】正确书写下列化学用语,并完成相应填空。
(1)3个钠离子________ ;
2个亚铁离子________ ;
氧化铁中氧显-2 价 ________;
4个氮分子________ ;
氦气________;
(2)能支持燃烧,供给人类呼吸的气体是________;
(3)食盐的主要成份是________ ;
(4)白磷在空气中燃烧的化学方程式是________;该反应的基本类型是 ________。
(5)将二氧化碳通入澄清石灰水中,石灰水变浑浊;该反应的化学方程式是________。
【答案】![]() 2Fe2+
2Fe2+ ![]() 4N2
4N2 ![]() O2 NaCl
O2 NaCl 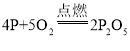 化合反应
化合反应 ![]()
【解析】
(1)离子的表示方法:在该离子元素符号的右上角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是在元素符号前面加上相应的数字。
钠离子对应的化合价为+1价,所以3个钠离子写为![]() ;
;
亚铁离子对应的化合价为+2价,所以2个亚铁离子写为2Fe2+;
氧化铁中的氧显-2价,元素化合价的表示方法是在化学式该元素的上方用正负号和数字表示,正负号标在数字前面。因此标成![]() ;
;
分子用化学式表示,多个分子就是在化学式前面加上相应的数字,故4个氮分子写成4N2;氦气是由原子构成的单质,故写成He。
(2)能支持燃烧,供给人类呼吸的气体是氧气,写成O2。
(3)食盐的主要成份是氯化钠,写成NaCl。
(4)白磷在空气中燃烧是磷与氧气反应生成五氧化二磷,因此化学反应方程式为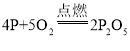 ,该反应符合“多变一”的特点,属于化合反应。
,该反应符合“多变一”的特点,属于化合反应。
(5)将二氧化碳通入澄清石灰水中,石灰水变浑浊,是二氧化碳与氢氧化钙反应生成了碳酸钙沉淀和水,化学反应方程式为![]() 。
。

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】为测定某石灰石矿中碳酸钙的含量,兴趣小组同学称取12.5g石灰石矿样品粉末于烧杯中,将80 g稀盐酸分四次加入,充分反应,测得实验数据如下表所示(杂质不溶于水,也不参与反应,生成的气体全部逸出):
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀盐酸的质量(g) | 20 | 20 | 20 | 20 |
烧杯中剩余物的质量(g) | 30.5 | 48.5 | 68.1 | 88.1 |
(1)样品完全反应生成二氧化碳的总质量为多少g。
(2)计算该石灰石矿中碳酸钙的质量分数。