题目内容
【题目】取含杂质的硫酸铜样品9g(杂质不溶于水,也不参加反应),向其中加入一定量的氢氧化钠溶液,恰好完全反应,得到沉淀和71 g溶质质量分数为10%的溶液。计算:
(1)样品中硫酸铜的质量;
(2)所加入的氢氧化钠溶液中溶质的质量分数(计算结果精确至0.1%);
【答案】(1)8 g ;(2)5.9%
【解析】
本题的反应是:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,最后得到的溶质是硫酸钠,其质量是71 g×10%=7.1g,将硫酸钠的质量待人方程式进行计算,求出NaOH、CuSO4、Cu(OH)2的质量,再利用:反应后溶液的质量=所有反应物质量之和![]() 沉淀及杂质,进行分析作答。
沉淀及杂质,进行分析作答。
解:反应后溶液中溶质硫酸钠的质量:71g×10%=7.1g;
设硫酸铜的质量为![]() ,氢氧化钠的质量为
,氢氧化钠的质量为![]() ,生成氢氧化铜的质量为
,生成氢氧化铜的质量为![]() ;
;
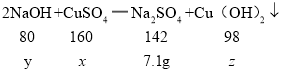
![]() ,解得
,解得![]() =8g
=8g
![]() ,解得
,解得![]() =4g
=4g
![]() ,解得
,解得![]() =4.9g
=4.9g
所加入的氢氧化钠溶液中溶质的质量分数为![]() 。
。
答:(1)样品中硫酸铜的质量为8 g;(2)所加入的氢氧化钠溶液中溶质的质量分数为5.9%。

练习册系列答案
相关题目