题目内容
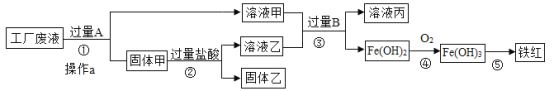
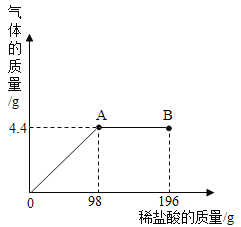
【题目】向盛有11.4gNa2CO3和Na2SO4的固体混合物的烧杯中,缓慢加入溶质质量分数为10%的稀硫酸,放出气体的总质量与所加入稀硫酸的质量关系如图10所示。请计算:
(1)生成二氧化碳的总质量为 。
(2)配制200g质量分数为10%的稀硫酸,需质量分数98%的浓硫酸 g。
(3)当加入稀硫酸至图中A点时,溶液中溶质的质量分数(烧杯中为不饱和溶液)。
【答案】(1)4.4g;(2)20.4;(3)14.3%
【解析】
碳酸钠与硫酸反应生成硫酸钠、水和二氧化碳,硫酸钠不与硫酸反应。
(1)由图可知,生成二氧化碳的质量为4.4g;
(2)200g质量分数为10%的稀硫酸中溶质质量为:200g×10%=20g;需质量分数98%的浓硫酸的质量为:20g÷98%≈20.4g;
(3)设固体混合物中碳酸钠的质量为x,生成硫酸钠的质量为y
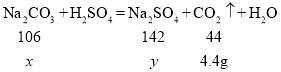
![]() x=10.6g
x=10.6g
![]() y=14.2g
y=14.2g
当加入稀硫酸至图中A点时,溶液中溶质的质量分数为:![]() 。
。
答:当加入稀硫酸至图中A点时,溶液中溶质的质量分数为14.3%。

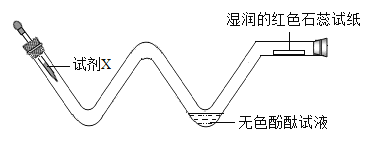
【题目】小明参观某养鱼池时,好奇地发现农民向养鱼池中撒一种叫做过氧化钙的淡黄色固体,用来增加鱼池中的含氧量。小明刚学完氧气的实验室制法,于是他想可否用过氧化钙制取氧气。
[提出问题] 过氧化钙可否用于制取氧气?
[查阅资料] 过氧化钙(CaO2)室温下稳定,300℃时分解成氧气,可做增氧剂、杀菌剂等。
[猜想与论证] (1)小明依据__________________,提出猜想Ⅰ。
猜想Ⅰ:用加热过氧化钙可制取氧气。
验证猜想Ⅰ是否正确的有关实验如下表,完成表中的空白处。
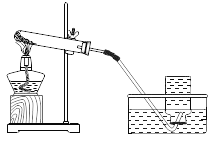
实验装置 | 实验主要过程 |
| ①检验装置气密性。操作如下:将导管伸入液面下,用手紧握试管,观察到_________,松开后,有液体进入导管; ②加入过氧化钙,加热,导管口有大量气泡冒出; ③收集一瓶气体。图示收集方法为______,能用该方法收集氧气的原因是_________; ④停止加热。熄灭酒精灯前,应_________; ⑤检验气体。方法是_________。 |
实验结论:通过上述实验证明,加热过氧化钙可制取氧气 | |
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ。
猜想Ⅱ:用过氧化钙与水反应可制取氧气。
验证猜想Ⅱ是否正确的有关实验如下面表格。
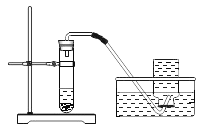
实验装置 | 实验主要过程 |
| ①检验装置气密性 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎看不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出 |
实验结论:通过上述实验证明,不能用过氧化钙与水反应制取氧气 | |
[分析与反思]:①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是_______________;②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?你的合理建议是_____________。(建议是否可行,还需进一步通过实验验证)。