题目内容
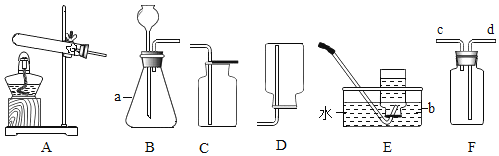
【题目】下列是初中化学中的一些常见实验。请回答:

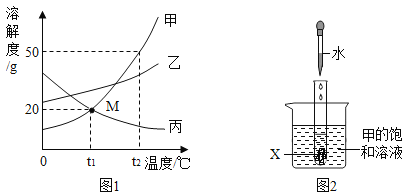
(1)图1是将纯铜片和黄铜片互相刻划,在纯铜片上有明显的划痕,这一实验现象说明________。
(2)图2是用![]() 试纸测小苏打溶液的酸碱度,若先用蒸馏水润湿
试纸测小苏打溶液的酸碱度,若先用蒸馏水润湿![]() 试纸,再滴小苏打溶液,则测得结果与实际值相比________(填“偏大”、“偏小”或“不变”)。
试纸,再滴小苏打溶液,则测得结果与实际值相比________(填“偏大”、“偏小”或“不变”)。
(3)图3是将等体积的水和氢氧化钠溶液分别倒入体积相同并充满![]() 的软塑料瓶中,迅速拧紧瓶盖,振荡,能说明
的软塑料瓶中,迅速拧紧瓶盖,振荡,能说明![]() 与氢氧化钠发生了化学反应的实验现象是________,
与氢氧化钠发生了化学反应的实验现象是________,![]() 与氢氧化钠反应的化学方程式是________。
与氢氧化钠反应的化学方程式是________。
【答案】黄铜比纯铜的硬度大(或合金比组成它的纯金属硬度大等合理表述) 偏小 倒入氢氧化钠溶液的软塑料瓶比倒入水的软塑料瓶变得更瘪等合理表述 ![]()
【解析】
解:(1)将纯铜片和黄铜片互相刻画,纯铜片上留下明显划痕,这一实验现象说明黄铜的硬度比纯铜大;
(2)用蒸馏水润湿,再把小苏打滴到试纸上,相当于稀释了小苏打,则会使小苏打的碱性变弱,由溶液的pH大于7时,呈碱性,且pH越小,碱性越弱,所以测得的结果与小苏打实际的pH比较偏小;
(3)图3是将等体积的水和氢氧化钠溶液分别倒入体积相同并充满CO2的软塑料瓶中,迅速拧紧瓶盖,振荡,能说明CO2与氢氧化钠发生了化学反应的实验现象是加入氢氧化钠的塑料瓶变瘪的程度严重,CO2与氢氧化钠反应生成碳酸钠和水,化学方程式是:CO2+2NaOH═Na2CO3+H2O。

 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案【题目】氯化铁(FeCl3)溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度氯化铁溶液的催化下,探究氯化铁对不同浓度过氧化氢溶液分解速率的影响。(资料:氯化铁溶液是氯化铁FeCl3和水的混合物,过氧化氢溶液是过氧化氢和水的混合物)
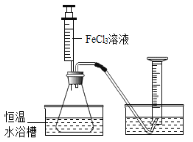
(1)分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的氯化铁溶液,如图所示,通过观察_______________可以粗略判断过氧化氢的分解速率,从而得出实验结果。
写出过氧化氢在氯化铁做催化剂时发生反应的文字表达式__________________。
(2)为进一步判断上述实验结论的准确性,小刚同学进行了如下实验方案设计:
[方案一] 在不同过氧化氢浓度下,测定收集相同气体所需时间。
[方案二] 在不同过氧化氢浓度下,测定____________________。
方案二的实验测量结果
过氧化氢溶液的浓度和体积 | 2%氯化铁溶液的体积(mL) | 反应的时间(min) | 生成O2的体积(mL) | |
实验1 | 8%10 mL | X | 5 | V1 |
实验2 | 16%10 mL | 3 | Y | V2 |
表中X=____________,Y=_____________。
实验结论:通过测量V1小于V2 ,说明_______________________。