题目内容
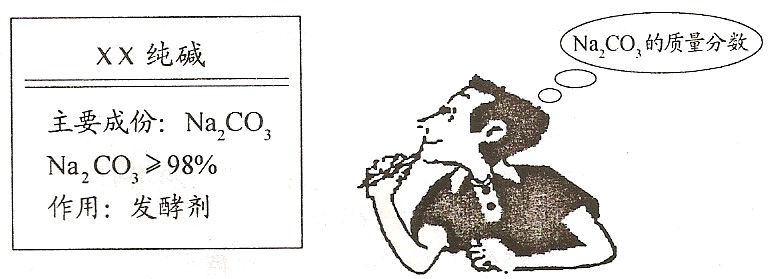
(3分) 星期天,小强的妈妈要焙制面包,叫小强去商店买回一包纯碱,小强仔细看了包装说明(如下图),并产生疑问:纯碱样品中碳酸钠的质量分数是否达标呢?
回到学校,他取出从家里带来的一小包纯碱样品和小明一起进行实验,小明和小强分别设计了以下两种不同的实验方案:
|
|
实验方案 |
|
小强 |
准确称取5.5 g纯碱样品放入烧杯中,又取来50克、14.6%的稀盐酸逐滴加入,至刚好不再产生气泡停止滴加稀盐酸,还剩余稀盐酸25克。 |
|
小明 |
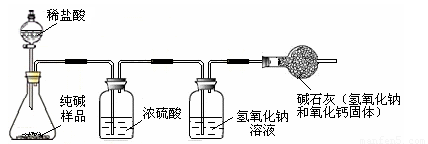
准确称取5.5 g纯碱样品放入锥形瓶中,加入一定质量分数、足量的稀盐酸,并将产生的气体干燥后通入足量的氢氧化钠溶液中(如下图所示) ,充分吸收后,称量氢氧化钠溶液质量增加了2.0克。
|
(1)小强测得的纯碱样品中碳酸钠的质量分数是多少?(写出计算过程)
(2)小明测得的纯碱样品中碳酸钠的质量分数是多少?(写出计算过程)
(3)两位同学又请来老师帮忙,老师选取另外一种测定方法经反复测定结果都是96.3%,请你结合实验过程分析一下两位同学谁的测定结果不准确,为什么?
(1)96.4% (2)87.6%
(3)小明的实验中产生的气体不能全部被氢氧化钠溶液吸收,残留在仪器中一部分,使得测定结果不准确。
【解析】
试题分析:根据化学方程式计算即可。
(1)解:设纯碱样品中碳酸钠的质量为x。
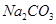 +2HCl="2NaCl+"
H2O+ CO2↑
+2HCl="2NaCl+"
H2O+ CO2↑
106 73
x 25g×14.6%
106:73=x:25g×14.6%
x=5.3g
纯碱样品中碳酸钠的质量分数是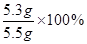 =96.4%。
=96.4%。
答:纯碱样品中碳酸钠的质量分数是96.4%。
(2)解:设纯碱样品中碳酸钠的质量为y。
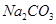 +2HCl="2NaCl+"
H2O+ CO2↑
+2HCl="2NaCl+"
H2O+ CO2↑
106 44
y 2.0g
106:44=y:2.0g
y=4.8g
纯碱样品中碳酸钠的质量分数是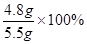 =87.6%。
=87.6%。
答:纯碱样品中碳酸钠的质量分数是87.6%。
(3)因为小明的实验中产生的气体不能全部被氢氧化钠溶液吸收,残留在仪器中一部分,使得测定结果不准确。
考点:根据化学方程式计算;实验设计与探究。
点评:根据化学方程式计算,要注意解题的步骤,设、写、找、列、解、答。
要想实验的结果准确,设计科学合理的实验很重要。

(3分) 星期天,小强的妈妈要焙制面包,叫小强去商店买回一包纯碱,小强仔细看了包装说明(如下图),并产生疑问:纯碱样品中碳酸钠的质量分数是否达标呢?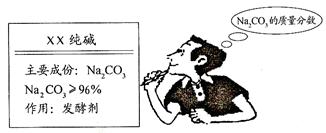
回到学校,他取出从家里带来的一小包纯碱样品和小明一起进行实验,小明和小强分别设计了以下两种不同的实验方案:
| | 实验方案 |
| 小强 | 准确称取5.5 g纯碱样品放入烧杯中,又取来50克、14.6%的稀盐酸逐滴加入,至刚好不再产生气泡停止滴加稀盐酸,还剩余稀盐酸25克。 |
| 小明 | 准确称取5.5 g纯碱样品放入锥形瓶中,加入一定质量分数、足量的稀盐酸,并将产生的气体干燥后通入足量的氢氧化钠溶液中(如下图所示) ,充分吸收后,称量氢氧化钠溶液质量增加了2.0克。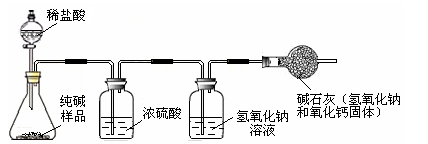 |
(2)小明测得的纯碱样品中碳酸钠的质量分数是多少?(写出计算过程)
(3)两位同学又请来老师帮忙,老师选取另外一种测定方法经反复测定结果都是96.3%,请你结合实验过程分析一下两位同学谁的测定结果不准确,为什么?