题目内容
【题目】下列是初中化学中的一些重要实验。请回答:
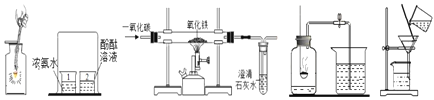
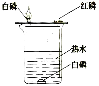
A B C D E F
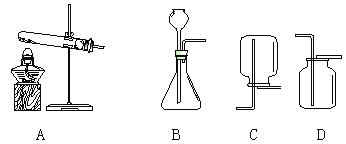
(1)A实验是铁丝在氧气中燃烧,可能导致的后果是________,改进措施是_____;
(2)B实验探究了分子的性质,一段时间后观察到的现象是_____,说明了______;
(3)C实验是一氧化碳还原氧化铁,实验开始时先__________后_________,硬质玻璃管中发生反应的化学方程式是__________,该装置的缺陷是____________;
(4)图D是利用红磷测定空气中氧气的含量实验,实验结束后,发现进入集气瓶中水的体积超过总容积的1/5,你认为导致这一结果的原因可能是__________(填序号)
a.实验前未将橡胶管夹紧 b.未等冷却就打开止水夹
c.实验前导管中未加满水 d.红磷的量不足
(5)C是过滤操作,其中玻璃棒的作用是___________,过滤后发现滤液仍然浑浊,其可能的原因是_____________(答出一种原因即可);
(6)F实验为探究燃烧的条件,其中热水的作用是____________、__________。
【答案】生成物溅落,集气瓶炸裂 集气瓶底部放少量水或细沙 酚酞溶液变红 微粒不断运动的 通一氧化碳 加热 3CO + Fe2O3 ![]() 2Fe + 3CO2↑ 没有进行尾气处理 a 引流 滤纸破损或漏斗内液面高于滤纸的边缘(合理即可) 隔绝氧气 提供温度或提供热量
2Fe + 3CO2↑ 没有进行尾气处理 a 引流 滤纸破损或漏斗内液面高于滤纸的边缘(合理即可) 隔绝氧气 提供温度或提供热量
【解析】
(1)铁丝在氧气中燃烧放出大量的热,使固体熔化为液体落到瓶底而炸裂集气瓶底,改进措施是在集气瓶底部放少量水或细沙。
(2浓氨水中的氨分子在不停地运动,一部分氨分子运动到烧杯2中,氨分子能使酚酞试液变红,该实验说明了微粒在不停地运动。
(3)C实验是一氧化碳还原氧化铁,实验开始时先通一氧化碳后加热,以防发生爆炸,一氧化碳与氧化铁在高温条件下发生反应生成铁和二氧化碳,该装置的尾气中含有有毒的一氧化碳,要燃烧掉或收集起来,以防污染空气。
(4)a.实验前未将橡胶管夹紧,红磷燃烧放出热量,气体膨胀,有部分气体逸散到空气中,导致进入集气瓶中水的体积超过总容积的![]() ,此选项符合题意;b.未等冷却就打开止水夹,导致进入集气瓶中水的体积少于总容积的
,此选项符合题意;b.未等冷却就打开止水夹,导致进入集气瓶中水的体积少于总容积的![]() ,此选项不符合题意;c.实验前导管中未加满水,等装置冷却后,只能使流入瓶内的水减少,使进入集气瓶中水的体积少于总容积的
,此选项不符合题意;c.实验前导管中未加满水,等装置冷却后,只能使流入瓶内的水减少,使进入集气瓶中水的体积少于总容积的![]() ,此选项不符合题意;d.红磷的量不足,消耗部分氧气,使进入的水偏少,此选项不符合题意。故选a。
,此选项不符合题意;d.红磷的量不足,消耗部分氧气,使进入的水偏少,此选项不符合题意。故选a。
(5)过滤操作中玻璃棒的作用是引流,过滤后发现滤液仍然浑浊,说明实验失败,其可能原因是滤纸破损或漏斗内液面高于滤纸的边缘。
(6)F实验为探究燃烧的条件,其中热水的作用是隔绝氧气、提供热量。

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案【题目】碳还原氧化铜的实验如右图所示。写出该反应的化学方程式____。
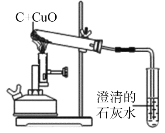
(提出问题)碳燃烧时可能生成CO2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
(作出猜想)猜想①:CO
猜想②:CO2
想③:____________。
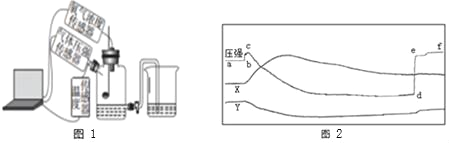
(设计方案)实验装置如图(浓硫酸具有吸水作用)。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通一段时间氮气。
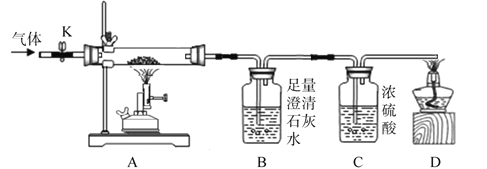
方案一:从定性观察角度判断
(1)实验时A处的现象是____________。
(2)若猜想①成立,B、D处的现象是_____________(填序号)。
a.B中变浑浊,D处能点燃 b.B中变浑浊,D处不能点燃
c.B中无明显实验现象,D处能点燃 d.B中无明显实验现象,D处不能点燃
方案二:从定量计算角度判断
取一定量炭粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:
反应前的质量 | 反应后的质量 | |
A(玻璃管+固体) | m1 | m2 |
B+C(广口瓶+混合液) | m3 | m4 |
(3)若猜想②成立,则理论上(m4-m3)__(m1-m2)(选填“<”、“>”或“=”)。
(4)若猜想③成立且CuO全部转化成Cu,则参加反应的碳的质量m的取值范围是____。
(交流反思)实验开始前缓缓通入氮气的目的是____。