题目内容
【题目】某化学小组在完成实验室制取CO2实验后,过滤得100g混合溶液,已知其中H+和Ca2+的个数比为2:1,为了弄清所得溶液的组成,向溶液中加入20g碳酸钠样品(所含杂质不溶于水,也不与其他物质反应),恰好完全反应后,过滤得到14.4g固体,求混合液中氯化氢和氯化钙的质量分数为
A.7.3% 11.1%B.3.65% 20%C.3.65% 5.55%D.7.3% 10%
【答案】C
【解析】
碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,反应的化学方程式及其质量关系:Na2CO3+2HCl=2NaCl+H2O+CO2↑,Na2CO3+CaCl2 ═CaCO3↓+2NaCl,由反应的化学方程式可知,每个碳酸钠“分子”和2个氯化氢“分子”恰好完全反应,和1个氯化钙“分子”恰好完全反应,即每个碳酸钠“分子”恰好完全反应时,消耗H+和Ca2+的个数比为2:1,说明碳酸钠一半和盐酸反应,一半和氯化钙反应。
解:设和氯化钙反应的碳酸钠质量为x,氯化钙的质量为y,生成碳酸钙沉淀的质量为z,
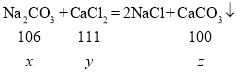
![]()
![]()
根据题意可知, ![]()
![]()
![]()
设氯化氢质量为m,
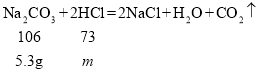
![]()
![]()
混合液中氯化氢和氯化钙的质量分数分别为:
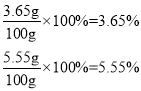
故选C。

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目