题目内容
【题目】科学方法对化学学习起着事半功倍的作用。分类归纳是研究化学物质重要的方法。如图是某位同学整理的铁及其化合物的知识网络图。
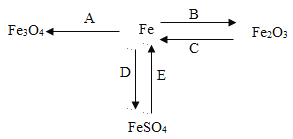
(1) A反应是铁丝燃烧的过程,生成黑色固体Fe3O4,计算该物质的相对分子质量_____;
(2)B反应是铁生锈的过程,铁锈(主要成分是Fe2O3) 疏松多孔,而金属铝比铁活泼却耐腐蚀,原因是(用文字描述)_____;
(3) C反应是炼铁过程,实验室常用一氧化碳来还原氧化铁。①硬质玻璃管中的现象是_____;反应的化学方程式为_____;实验开始前要先通一段时间气体再加热的原因是_____;②中装满混合液(过量的氢氧化钠和氢氧化钙混合液,氢氧化钠吸收二氧化碳能力比氢氧化钙强),则虚线框内装置的作用是_____(填字母序号)。
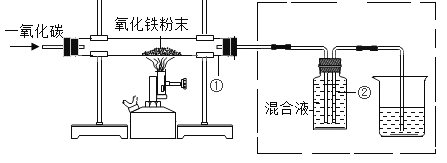
a. 收集二氧化碳
b.检验二氧化碳
c.收集一氧化碳
(4)D反应是金属铁与稀硫酸的反应,实验现象为_____;
(5)D反应是现代湿法冶金的先驱,写出其化学反应方程式_____;该反应说明金属活动性:Fe_____Cu (填 “>”“<”“=”)
(6)与FeSO4中铁元素的化合价相同的铁的氧化物的化学式是_____。
【答案】232 金属铝表面可形成致密的氧化铝薄膜,对内部的铝有保护作用 红色固体逐渐变为黑色 ![]() 赶出装置内的空气,防止加热爆炸 bc 固体溶解并有气体生成,同时溶液由无色变浅绿色
赶出装置内的空气,防止加热爆炸 bc 固体溶解并有气体生成,同时溶液由无色变浅绿色 ![]() > FeO
> FeO
【解析】
(1)Fe3O4的相对分子质量为![]()
(2)铝的活动性强于铁,但铝被氧化后在表面可形成致密的氧化铝薄膜,阻止内层金属继续被氧化,因此铝的耐腐蚀性强于铁;
(3)一氧化碳还原氧化铁的现象是红色固体逐渐变黑,方程式为![]() ;因为一氧化碳为可燃性气体,与空气混合后加热很不安全,故先通入CO赶出装置内的空气,防止加热爆炸;虚线框中混合液可以吸收并验证CO2,而CO不溶于水和碱,可排出混合液,收集未反应的CO;
;因为一氧化碳为可燃性气体,与空气混合后加热很不安全,故先通入CO赶出装置内的空气,防止加热爆炸;虚线框中混合液可以吸收并验证CO2,而CO不溶于水和碱,可排出混合液,收集未反应的CO;
(4)D反应是铁和稀硫酸反应生成硫酸亚铁和氢气,现象是固体溶解并有气体生成,同时溶液由无色变浅绿色;如果Fe→FeSO4是湿法冶金,则是铁与硫酸铜反应生成硫酸亚铁和铜,方程式![]() ,该反应说明Fe的金属活动性大于Cu;
,该反应说明Fe的金属活动性大于Cu;
(5)FeSO4中铁为+2价,则+2价铁的氧化物化学式为FeO;
故答案为:232;金属铝表面可形成致密的氧化铝薄膜;红色固体逐渐变为黑色;![]() ;赶出装置内的空气,防止CO爆炸;bc;固体溶解并有气体生成,同时溶液变浅绿色;
;赶出装置内的空气,防止CO爆炸;bc;固体溶解并有气体生成,同时溶液变浅绿色;![]() ;>;FeO。
;>;FeO。

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案