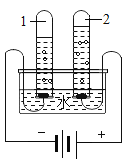
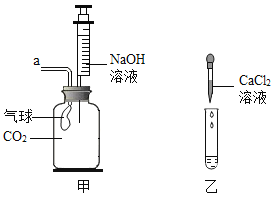
��Ŀ����
����Ŀ��������ͼ�ش����⣺
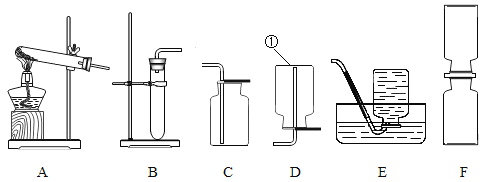
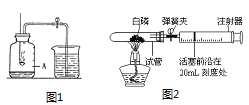
��1��д��ͼ�б��������������__��
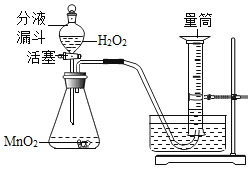
��2��ʵ������п����ϡ������ȡ���ռ��ϴ�����������Ӧѡ�õ�װ����__������ţ���ͬ������Ӧ�Ļ�ѧ����ʽ��__��
��3����֪ͭ��Ũ���ᷴӦ������ȡ�����������壬����������һ�ֺ���ɫ�����壬�ܶȱȿ�����
����ȡ��������Ӧѡ�õķ���װ����__����ͭƬ�����Թ��е���ȷ������__��
����ͼ��Fװ������ʾ�����˶���ʵ��ʱ��Ϊ��������ʾ��ʱ�䣬NO2��÷���__����������������������ļ���ƿ�У���һƿ�ǿ�������ȥ��ƿ֮��IJ���Ƭ�����Կ�����������__��
���𰸡�����ƿ BE Zn+H2SO4�TZnSO4+H2�� B ���Թܺ�ţ������Ӽг�ͭƬ�����Թܿڣ����������Թܣ� �� �ϲ㼯��ƿ�еĺ���ɫ�������²㼯��ƿ����ɢ���������²㼯��ƿ�г�����ɫ��ͬ�����壮
��������
��1������������������Ǽ���ƿ���������ռ����壮
�������ƿ��
��2��ʵ������п����ϡ������ȡ��������Ҫ���ȣ�Ӧ����Bװ����Ϊ����װ�ã�
�������ܶȱȿ���С�������������ſ������ռ�������Dװ���ռ�������������ˮ����������ˮ���ռ�������Eװ���ռ�������ˮ���ռ������������ſ������ռ�������������
п��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��Zn+H2SO4�TZnSO4+H2����
���BE�� Zn+H2SO4�TZnSO4+H2����
��3������ȡ��������ʱ����Ҫ���ȣ�Ӧѡ�õķ���װ����Bװ�ã�
��ͭƬ�����Թ��е���ȷ�����ǰ��Թܺ�ţ������Ӽг�ͭƬ�����Թܿڣ����������Թܣ�
���B�����Թܺ�ţ������Ӽг�ͭƬ�����Թܿڣ����������Թܣ�
����ͼ��Fװ������ʾ�����˶���ʵ��ʱ��Ϊ��������ʾ��ʱ�䣬���ڶ����������ܶȱȿ�������ðѶ������������ϲ�ļ���ƿ�У���һƿ�ǿ�������ȥ��ƿ֮��IJ���Ƭ�����Կ������������ϲ㼯��ƿ�еĺ���ɫ�������²㼯��ƿ����ɢ���������²㼯��ƿ�г�����ɫ��ͬ�����壮
����ϣ��ϲ㼯��ƿ�еĺ���ɫ�������²㼯��ƿ����ɢ���������²㼯��ƿ�г�����ɫ��ͬ�����壮

����Ŀ��С����С����ʵ�����������ʯ��ʯ��Ӧ���ֱ��üס���װ��(�����Ծ�����)���ж�����̼����ȡ������ʵ�飬����δ���ֳ���ʯ��ˮ���ǣ���Դ�����ͬѧ��������Լ����뷨��
С��ͬѧʵ��ʱ����ʯ��ˮδ����ǵ�ԭ����_______��
��������⣩С��ͬѧʵ��ʱ����ʯ��ˮΪʲôû�б�����أ�
���������룩����һ������ʯ��ˮ���ʣ����������Ӧ��������������ж�����̼�⣬�����Ȼ��⣮
���������ϣ��Ȼ�����������ˮ�γ����ᣮ
��ʵ��̽����
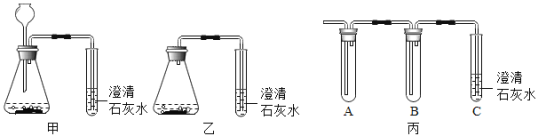
ʵ�� | ʵ�鲽�� | ʵ������ | ʵ����� |
ʵ���� | ��������CO2ͨ�뵽��ʵ�����õij���ʯ��ˮ�� | �����ʯ��ˮ���� | ����һ������ |
ʵ���� | ����Ӧ����������ͨ�뵽_____ | _____ | ��������� |
ͬѧ�Ǿ������۷��֣��ñ�װ��(��ͼ)��A��B�о�����ʵ���������Լ�����ͬʱ����������������̽��������Bװ�������������_____���������____�������������붼������
��ʵ�鷴˼����ʵ���֪��С��ͬѧʵ��ʱ���ܴ���ʹ����һ��ҩƷ����ʹ�õ�ҩƷ��___��
����Ŀ���ڸ����£�����ˮ�����ܷ�����Ӧ����һ�ֳ��������������һ�����壬ij��ѧ ѧϰС���ͬѧ�Դ˷�Ӧ˦����Ȥ����С�鼯��Э�������������ʵ�飬��̽��������ˮ������Ӧ��IJ��Ҳ������һ�����������̽����
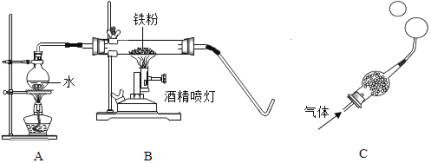
(1)Aװ�õ�������___��
(2)̽�����ɵ�������ʲô��
����������裩����һ�����ɵ����������������
����������ɵ����������������
��ʵ��̽���������ɵ�����ͨ��Cװ�ã����ι���װ�м�ʯ�Ҹ���������ܿ�պЩ����ˮ(��ϴ�Ӽ���Һ)�������������٣����������ݣ��������ݴ���һ����ʱ������ڶ����ܣ�����������ܿں�������������ȼ�ŵ�ľ�����������ݣ��б�������
���ƶϣ����ɵ�������___��
(3)̽���Թ���ʣ�����ɷ���ʲô��
���������ϣ�
�������������� | FeO | Fe2O3 | Fe3O4 |
��ɫ��״̬ | ��ɫ��ĩ | ����ɫ��ĩ | ��ɫ���� |
�ܷ��������� | �� | �� | �� |
�ܷ������ᷴӦ | �� | �� | �� |
��������֤���Թ���ʣ�����Ϊ��ɫ����ȫ��������������
����������裩����һ��ʣ�������Fe��Fe3O4��
�������ʣ������ǣ�___��
��ʵ��̽����
ʵ����� | ʵ�������� |
____ | _____ |
[ʵ�����]����ˮ������Ӧ�Ļ�ѧ����ʽΪ��___��
����˼�뽻�����ú�ɫ���岻������FeO��Fe2O3��������___��