题目内容
【题目】金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)如图是铝的原子结构示意图。下列说法不正确的是______。
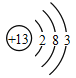
A铝原子的质子数为13
B在化合物中铝通常显+3价
C铝是地壳中含量最多的元素
D铝可作导线是由于它具有良好的导电性
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了如图实验, 并对溶液A和固体B的成分进行了分析和实验探究。
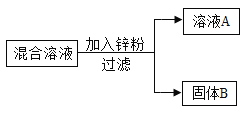
(提出问题)溶液A中的溶质可能有哪些?
(作出猜想)①只有Zn(NO3)2;②Zn (NO3)2、AgNO3;③Zn (NO3)2、Cu(NO3)2;④Zn (NO3)2、AgNO3、Cu(NO3)2
(交流讨论)不合理的猜想是__________(填标号),其理由是_________________。
(实验探究)若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤 | 现象 | 有关反应的化学方程式 |
取少量固体B,滴加________________ | 有气泡产生 | ____________________ |
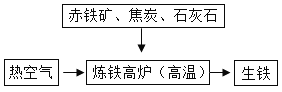
(3)如图是工业炼铁示意图。其中,焦炭的作用是燃烧提供能量和_______________;有铁生成的化学方程式为________________。
(4)若73 g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数__________。
【答案】C ② 锌先于硝酸银溶液反应,如果溶液中有硝酸银,说明硝酸铜还没开始反应,溶液中一定含有硝酸铜 稀盐酸 Zn+2HCl═ZnCl2+H2↑ 做还原剂制取一氧化碳 Fe2O3+3CO![]() 2Fe+3CO2 11.7%
2Fe+3CO2 11.7%
【解析】
(1)A、根据原子结构示意图的特点可知:铝的核内质子数为13,故A正确;
B、根据原子的核外电子在化学反应中的规律特点可知:铝的最外层电子数是3,且在化学反应中易失掉3个电子而达到稳定结构,在化合物中铝通常显+3价,故B正确;
C、依据地壳中元素的含有情况可知,铝是地壳中含量最多的金属元素,而含量最多的元素是氧;故C错误;
D、根据金属铝的性质可知:铝具有较好的导电性,所以可以用铝制作导线;故D正确;
故选:C;
(2)[交流讨论]锌加入到AgNO3和Cu(NO3)2混合溶液中,锌先于硝酸银溶液反应生成银和硝酸锌,硝酸银反应完全后,锌再与硝酸铜反应,如果溶液中有硝酸银,说明硝酸铜还没开始反应,溶液中一定含有硝酸铜;所以猜想②是错误的;故填:②;锌先于硝酸银溶液反应,如果溶液中有硝酸银,说明硝酸铜还没开始反应,溶液中一定含有硝酸铜;
[实验探究]如果猜想①成立说明锌把硝酸银、硝酸铜都反应完了,根据实验现象可以知道应该加入稀盐酸,同时可以判断出锌是过量的,所发生的反应为锌和稀盐酸的反应,反应物是锌和盐酸,生成物是氯化锌和氢气,该反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑.
故填:稀盐酸;Zn+2HCl═ZnCl2+H2↑;
(3)图中是工业炼铁示意图,其中,焦炭的作用是燃烧提供能量和做还原剂制取一氧化碳;一氧化碳和氧化铁反应生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
故填:做还原剂;Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(4)设反应后生成氯化钠的质量为x
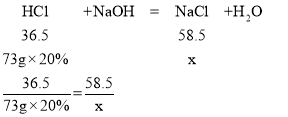
x=23.4 g
反应后所得溶液的质量分数为:![]() ×100%═11.7%
×100%═11.7%
答:反应后所得溶液的质量分数为11.7%。

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案【题目】长久使用热水壶底部有层水垢,主要成分为CaCO3和Mg(OH)2,某学校化学研究小组的同学通过实验测定水垢中CaCO3的含量:将过量的稀盐酸加入到200g水垢中,把产生的CO2气体用足量的NaOH溶液吸收,同时测量3min钟内NaOH溶液增加的质量,结果如下表:
时间/s | 0 | 30 | 60 | 90 | 120 | 150 | 180 |
质量/g | 0 | 30 | 50 | 60 | 66 | 66 | 66 |
(1)写出CO2被足量的NaOH溶液吸收时,发生的化学反应方程式_______________。
(2)从表格中可以看出,200g水垢与盐酸反应生成的CO2最多是___________g。
(3)计算水垢中碳酸钙的质量分数,写出计算过程_________