题目内容
【题目】科技推动着奥林匹克运动的发展,在奥运会中化学的表现十分突出。

(1)“鸟巢”的建造中使用了大量的钢铁。生产这些钢铁时要在高温条件下将Fe2O3用一氧化碳还原成铁,其反应的化学方程式为________________________。
(2)“水立方”的膜结构是由化学合成材料ETFT制成的,化学式是(C2H2F2)n则ETFT中C、H、F的质量比是________, C的质量分数是________。
(3)撑杆跳高使用的玻璃纤维杆,其主要成分是SiO2、Al2O3等,在物质分类中它们属于________(填序号)。 A.单质 B.化合物 C.氧化物
【答案】 Fe2O3+3CO![]() 2Fe+3CO2 12:1 37.5% BC
2Fe+3CO2 12:1 37.5% BC
【解析】(1)氧化铁和一氧化碳反应生成铁和二氧化碳的化学方程式为:Fe2O3+3CO![]() 2Fe+3CO2;(2)化合物中元素的质量比=(相对原子质量×原子个数)之比,
2Fe+3CO2;(2)化合物中元素的质量比=(相对原子质量×原子个数)之比, ![]() ;(C2H2F2)n中C、H、F的质量比是12×2:1×2=12:1, C的质量分数是:12×2÷(12×2+1×2+19×2)×100%=37.5%;(3)二氧化硅、氧化铝都是由不同元素组成的纯净物,是化合物;都是由氧元素和另外一种元素组成的化合物,属于氧化物。故填:BC。
;(C2H2F2)n中C、H、F的质量比是12×2:1×2=12:1, C的质量分数是:12×2÷(12×2+1×2+19×2)×100%=37.5%;(3)二氧化硅、氧化铝都是由不同元素组成的纯净物,是化合物;都是由氧元素和另外一种元素组成的化合物,属于氧化物。故填:BC。

 阶梯计算系列答案
阶梯计算系列答案【题目】小明向氢氧化钠溶液中滴加了稀盐酸,发现没有明显现象。为了判断两者是否恰好完全反应,他取少量反应后的溶液加入试管中,滴加几滴无色酚酞试液,振荡后观察到酚酞试液不变色。
(1)根据上述现象,小明得出“两种物质恰好完全反应”的结论。小白认为小明的结论是不合理的,其理由是____。
(2)小白利用pH试纸测反应后溶液的pH,以确定两者是否恰好完全反应。请你选用其他试剂再设计一个实验,以验证氢氧化钠和盐酸是否恰好完全反应(要求写出选用的试剂、可能观察到的现象和相应的结论):_____________________。
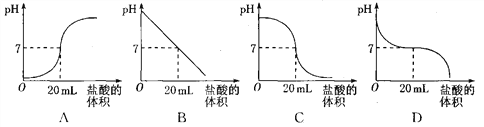
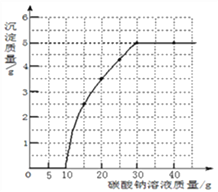
(3)小白为了继续探究“在氢氧化钠与盐酸反应的过程中,溶液的pH是如何变化的” 这一问题,进行如下实验:在一定量的氢氧化钠溶液中逐渐滴加盐酸,用pH试纸 测定溶液的pH,记录数据如下表。
盐酸的体积/mL | 0 | 10 | 19.5 | 20 | 20.5 | 30 | 40 |
pH | 13 | 12 | 11 | 7 | 3 | 2 | 1 |
下图中能合理表示该反应过程中pH变化的图像是________(填序号)。