题目内容
【题目】某同学用微型实验装置(如图)制取二氧化碳并检验其性质,回答问题。
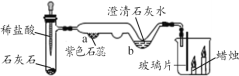
(1)试管中发生反应的化学方程式是______。
(2)b处出现的现象是_________。
(3)根据烧杯中的变化现象,得出二氧化碳的化学性质是______。
(4)另一同学操作时,误将浓盐酸当作稀盐酸使用,结果______处没有明显现象。
(5)你认为微型实验的优点是____(写一条即可)。
【答案】CaCO3+2HCl===CaCl2+H2O+CO2↑ 澄清的石灰水变浑浊 CO2不能燃烧也不支持燃烧 b 节约试剂、装置简单、减少污染、操作简便、安全可靠、效果良好(写出一条即可)
【解析】
(1)试管中碳酸钙和稀盐酸发生反应生成氯化钙、水和二氧化碳,化学方程式是CaCO3+2HCl===CaCl2+H2O+CO2↑;
(2)产生的二氧化碳能使澄清的石灰水变浑浊,故b处出现的现象是澄清的石灰水变浑浊;(3)烧杯中的阶梯蜡烛下面的先熄灭,上面的后熄灭,说明二氧化碳具有不燃烧不能支持燃烧的化学性质;
(4)浓盐酸具有挥发性,挥发出溶质氯化氢,会使二氧化碳中含有氯化氢,与石灰水接触,则氯化氢与氢氧化钙反应,看不到b处变浑浊的现象;
(5)该微型实验的优点是节约药品。

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案【题目】小军同学准备通过实验证明“二氧化锰能加快氯酸钾分解”。他设计了下表所示的探究实验,请你帮他完成下面未填完的空格
实验操作 | 实验现象 | 实验结论或总结 | ||
结论 | 总结 | |||
实验一 | 加热试管中少量氯酸钾,熔融时,伸入带火星的木条 | 带火星的木条复燃 | 加热氯酸钾能产生氧气,但是反应所需温度_________。 | 二氧化锰能加快氯酸钾分解 |
实验二 | 取少量二氧化锰于试管中,加热,伸入带火星的木条 | 没有明显现象 | ________________ | |
实验三 | _________________, 加热,伸入带火星的木条。 | ______ | 二氧化锰能加快氯酸钾的分解,反应的化学方程式为: ______________。 | |
(1)在小军的探究实验中,“实验一”和“实验二”起的作用是_________。
(2)小英同学认为上面的实验还不能证明二氧化锰是氯酸钾分解反应的催化剂,请你帮她写上理由___。