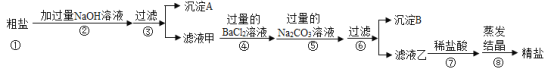
��Ŀ����
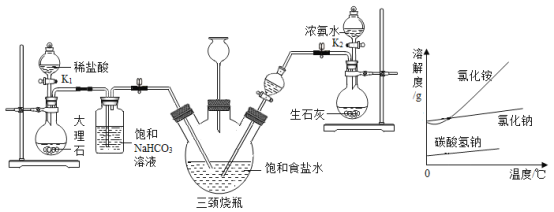
����Ŀ��������ĸA~F��ʾ���л�ѧ���������ʣ��������⡢̼�������ȡ��ơ��������е�2~3��Ԫ����ɡ�
��1��A����Ҫ�Ļ���ԭ�ϣ���������ֽ�����������Լ�ӡȾ�ȣ�Ҳ�Ǽ�ͥ�����г������ʣ���A���׳���______��
��2����ɫ��ĩB������C��Ӧ�õ���ɫ��ĩ����ѧ����ʽΪ__________________��
��3����D��E��Ӧ����������ά�������������������������ʡ���D��Һ�еμ�2-3����ɫʯ����Һ���ɹ۲쵽��Һ�������μ�E��Һ����Һ��죬��D��______���� ʱ��Һ�е�������______��
��4��F�������������й㷺��;�������ڸ��������������к����Է�ˮ�ȣ���F��A������Ӧ�Ļ�ѧ����ʽΪ_______________��
���𰸡��մ Fe2O3+3CO![]() 2Fe+3CO2 NaOH HCl��NaCl Na2CO3+Ca(OH)2=CaCO3��+2NaOH
2Fe+3CO2 NaOH HCl��NaCl Na2CO3+Ca(OH)2=CaCO3��+2NaOH
��������
A��F��ʾ���л�ѧ���������ʣ��������⡢̼�������ȡ��ơ��������е�2��3��Ԫ����ɣ�
��1��A����Ҫ�Ļ���ԭ�ϣ���������ֽ�����������Լ�ӡȾ�ȣ�Ҳ�Ǽ�ͥ�����г������ʣ�����A��̼���ƣ��׳��մ��
��2����ɫ��ĩB������C��Ӧ�õ���ɫ��ĩ�ķ�Ӧ����������һ����̼�ڸ��µ��������������Ͷ�����̼����ѧ����ʽΪ��Fe2O3+3CO![]() 2Fe+3CO2��
2Fe+3CO2��
��3��D��E��Ӧ����������ά�������������������������ʣ�����D��E���������ƺ����ᷴӦ�����Ȼ��ƺ�ˮ����D��Һ�еμ�2-3����ɫʯ����Һ���ɹ۲쵽��Һ�������μ�E��Һ����Һ��죬����D���������ƣ�E�����ᣬ����D��NaOH����ʱ��Һ�е�������HCl��NaCl��
��4��F�������������й㷺��;�������ڸ��������������к����Է�ˮ�ȣ�����F���������ƣ�F��A�����ķ�Ӧ���������ƺ�̼���Ʒ�Ӧ����̼��Ƴ������������ƣ���ѧ����ʽΪ��Na2CO3+Ca��OH��2�TCaCO3��+2NaOH��

����Ŀ�������ĸ�ͼ���У�����ȷ��ӳ��Ӧ�仯��ϵ����
|
|
|
|
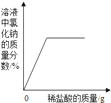
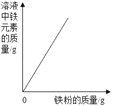
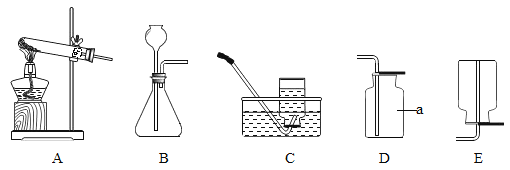
A����һ����������������Һ�еμ�ϡ���� | B����һ������ϡ�����м������ʯ | C��һ������ϡ�����м������� | D������һ�����ĸ�����ع��� |
A. A B. B C. C D. D
����Ŀ���±���NaC1��NH4Cl�ڲ�ͬ�¶�ʱ���ܽ�ȣ���ش�����
�¶ȣ��棩 | 10 | 20 | 30 | 40 | 50 | 60 | |
�ܽ�ȣ�g�� | NaC1 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 |
NH4C1 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
��1��30��ʱ��NaC1�����������������ֵ��_____��
��2��NaC1��NH4C1�ܽ�����ʱ����Ӧ�¶ȵ���С��ΧΪ_____��
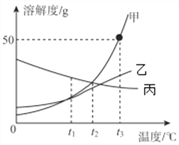
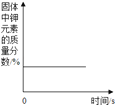
��3����ͼ��ʾ��A��60��ʱ����120gˮ��NH4C1��Һ��������ͼ�����õ����塣
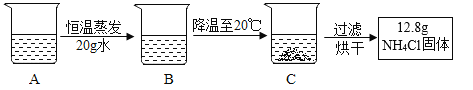
C����Һ������_____g��A��ҺΪNH4C1��_____��ѡ��������������������������Һ��