��Ŀ����
����Ŀ���ҹ�ú̿��Դ�ḻ��ú������ȼ���⣬������Ҫ�Ļ���ԭ�ϡ���ҵ����ú�Ϳ���Ϊԭ����������[CO��NH2��2]��һ���������£�
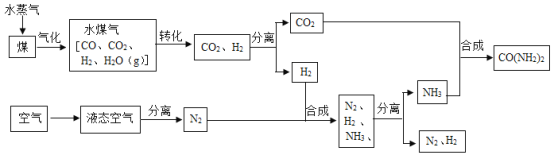
��1����Һ̬�����з����N2�Ĺ�������_____�����������ѧ�����仯��
��2����ú��ˮ������Ӧǰ���Ƚ�ú���飬��������Ŀ����_____��
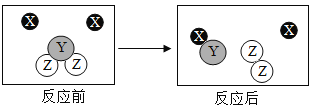
��3�����������з�������Ҫ��ӦΪ��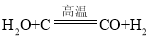 ��
��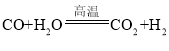 �����������û���Ӧ����_____����١��ڡ�������Ӧ������Ԫ�صĻ��ϼ۱仯Ϊ+1��0��̼Ԫ�صĻ��ϼ۱仯Ϊ_____����Ӧ���з�����ԭ��Ӧ��������_____��д��ѧʽ����
�����������û���Ӧ����_____����١��ڡ�������Ӧ������Ԫ�صĻ��ϼ۱仯Ϊ+1��0��̼Ԫ�صĻ��ϼ۱仯Ϊ_____����Ӧ���з�����ԭ��Ӧ��������_____��д��ѧʽ����
��4���ڸ��¸�ѹ�£�CO2��NH3���Ժϳ����أ�ͬʱ����ˮ���ɣ��÷�Ӧ�Ļ�ѧ����ʽΪ��_____��
��5��ʵ�������У�N2��H2������ȫ��ת��ΪNH3�����������п���ѭ�����õ������У�_____��
���𰸡����� ����ú����ˮ�����ĽӴ������ʹ��Ӧ����� �� 0��+2 H2O CO2��2NH3![]() CO(NH2)2��H2O ����������
CO(NH2)2��H2O ����������
��������
��1����Һ̬�����н��¡���ѹ�����N2�Ĺ�������û�������ʲ��������������仯��
��2����ú��ˮ������Ӧǰ���Ƚ�ú���飬��������Ŀ���ǣ�����ú����ˮ�����ĽӴ������ʹ��Ӧ����֣�
��3�����������з�������Ҫ��ӦΪ��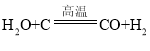 ��
��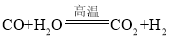 �����������û���Ӧ���Ǣ٣����ϡ�����+������=�µ���+�»��������Ӧ������Ԫ�صĻ��ϼ۱仯Ϊ+1��0��̼Ԫ�صĻ��ϼ۱仯Ϊ0��+2����Ӧ����ˮ�е�������ȥ��������������������ԭ��Ӧ��������ˮ��H2O��
�����������û���Ӧ���Ǣ٣����ϡ�����+������=�µ���+�»��������Ӧ������Ԫ�صĻ��ϼ۱仯Ϊ+1��0��̼Ԫ�صĻ��ϼ۱仯Ϊ0��+2����Ӧ����ˮ�е�������ȥ��������������������ԭ��Ӧ��������ˮ��H2O��
��4���ڸ��¸�ѹ�£�CO2��NH3���Ժϳ����أ�ͬʱ����ˮ���ɵĻ�ѧ����ʽΪ��CO2��2NH3![]() CO(NH2)2��H2O��
CO(NH2)2��H2O��
��5��ʵ�������У�N2��H2������ȫ��ת��ΪNH3��ÿ�κϳɰ�ʱ������ʣ�࣬�������������Ǻϳɰ���ԭ�ϣ����������п���ѭ�����õ������У�������������

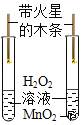
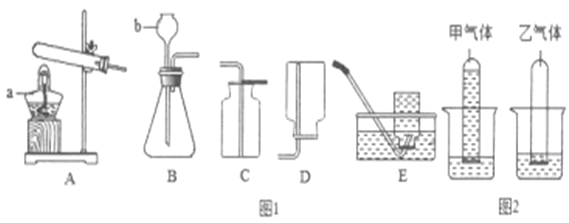
����Ŀ����ʵ��������÷ֽ����������Һ����������ػ���������ȡ������ij��ѧ��ȤС���������ʵ�����Ʒ�������̽����

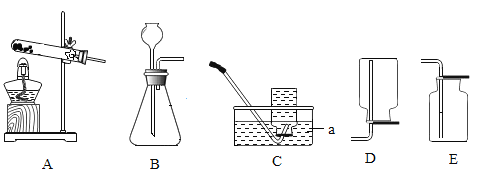
��1��С��ͬѧѡ����ͼ��ʾ��װ����ȡ��������д��ͼ�б������������A��_____B��_____����ȡ�������������Ļ�ѧ��Ӧ����ʽΪ��_____��ʵ��ǰС��ͬѧ��������A�м���ˮ��Ȼ�����ܷ���ˮ���У���������A�Ļ������۲쵼���ܿ��Ƿ������������ݳ��֣���ʵ�������Ŀ����_____��
��2��С��ͬѧͨ����������֪��CuSO4��Һ������ijЩ�����к��е����ʵ��ܴ���������ķֽ⣮���������к��й�������ø���ܴ���������ֽ⣬��������ø��_____��ѡ�������գ��������ࡢ�ڵ����ʡ���֬������ά���أ���ʵ��֤�����ڹ���������Һ�еμ�CuSO4��Һ�������ӿ��������ķֽ⣮CuSO4��Һ��Ҫ�����������ӣ�H2O��Cu2+��SO42������Ϊ�˽�һ��̽��CuSO4��Һ������������������ã�С��ͬѧ�������·�������ơ�
��С��ͬѧ��Ϊ����ܵ���H2O������������_____��
��Ҫ˵����������������Ƿ������ã�С��ͬѧ���������ʵ�飬��������̽�����
ʵ�鲽�� | ʵ������ | ���� |
a��ȡһ֧�Թܼ���5mL5%����������Һ��Ȼ�����2��3��ϡ���� | ��Һ����û�����ݷų� | ʵ��֤����������õ���_____�� |
b����ȡһ֧�Թܼ���5mL5%����������Һ��Ȼ�����2��3��_____��Һ | ��Һ���д������ݷų� |
����Ŀ������ʵ�鷽�����ܴﵽ��Ӧʵ��Ŀ�ĵ��ǣ�������
|
|
|
|
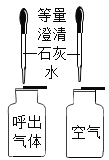
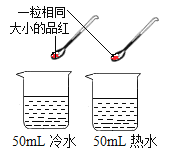
A֤�������к�����Ԫ�� | B֤����������Ⱥ�������е�CO2������ | C֤�����������ǹ�������ֽ�Ĵ��� | D֤���¶�Խ�ߣ������˶�����Խ�� |
A.AB.BC.CD.D