题目内容
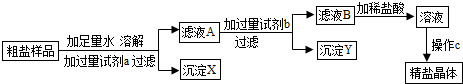
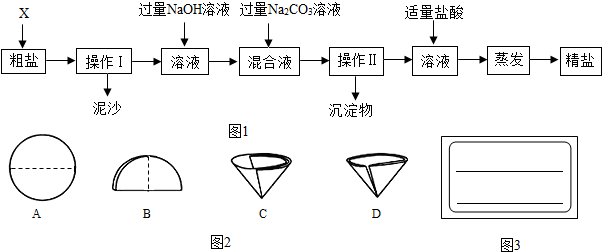
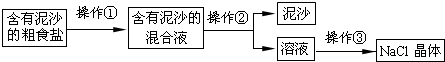
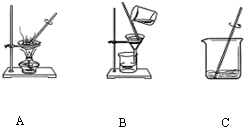
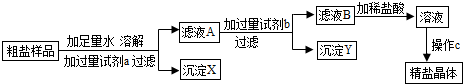
某粗盐溶液中,含有少量的氯化钙、氯化镁、硫酸钠和泥沙.进行以下操作可将杂质除去:①过滤;②加适量盐酸;③加过量氢氧化钠溶液;④加过量碳酸钠溶液;⑤加适量氯化钡溶液.正确的操作顺序是( )
| A.⑤④③①② | B.①②③④⑤ | C.①⑤④②③ | D.⑤③④②① |
A、加入适量的氯化钡溶液,可以将硫酸根离子转化为沉淀,加过量碳酸钠溶液,可以将钙离子和反应剩余的钡离子转化为沉淀,加过量氢氧化钠溶液,可以将镁离子转化为沉淀,过滤可以将沉淀和泥沙除去,加适量盐酸,可以除去反应剩余的碳酸根离子和氢氧根离子,最后的溶液中就只剩下了氯化钠和水,故A正确,
B、过滤只会将泥沙除去,而后面步骤中的沉淀是无法从溶液中除去的,故B错误,
C、过滤只会将泥沙除去,而后面步骤中生成的沉淀是无法从溶液中除去的,也就多达不到除杂的目的,故C错误,
D、加入适量的氯化钡溶液,可以将钡离子转化为沉淀,加过量氢氧化钠溶液,可以将镁离子转化为沉淀,加过量碳酸钠溶液,可以将钙离子和反应剩余的钡离子转化为沉淀.若先加入盐酸,会导致生成的沉淀溶解掉,所以本选项不能得到纯净氯化钠.故D错误.
故选A.
B、过滤只会将泥沙除去,而后面步骤中的沉淀是无法从溶液中除去的,故B错误,
C、过滤只会将泥沙除去,而后面步骤中生成的沉淀是无法从溶液中除去的,也就多达不到除杂的目的,故C错误,
D、加入适量的氯化钡溶液,可以将钡离子转化为沉淀,加过量氢氧化钠溶液,可以将镁离子转化为沉淀,加过量碳酸钠溶液,可以将钙离子和反应剩余的钡离子转化为沉淀.若先加入盐酸,会导致生成的沉淀溶解掉,所以本选项不能得到纯净氯化钠.故D错误.
故选A.

练习册系列答案
相关题目