题目内容
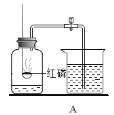
【题目】某干燥剂含有CaO、NaOH和CaCl2中的两种物质,为探究其成分,设计如图所示实验。依据实验流程回答相关问题。
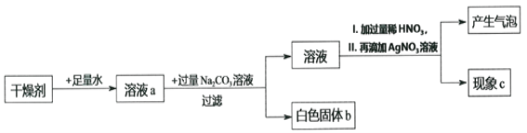
(1)溶液a一定显________性。
(2)白色固体b一定是_______(填化学式)。
(3)加入过量的稀HNO3的目的是_____________________。
(4)现象c:①若无白色沉淀,干燥剂成分为_________________。
②若有白色沉淀,干燥剂成分为___________________。
(5)稀HNO3溶液能否用稀HCl溶液替代_________________(填“能”或“不能”)。
【答案】碱 CaCO3 完全除去NaOH、Na2CO3,以免干扰检验CaCl2 CaO和NaOH CaO、CaCl2或NaOH、CaCl2 不能
【解析】
(1)溶液a和碳酸钠反应会生成白色沉淀,且干燥剂含有CaO、NaOH和CaCl2中的两种物质,所以溶液a中一定含有氢氧化钙,溶液显碱性;
(2)根据氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,则白色沉淀为CaCO3;
(3)检验氯离子,加硝酸银之前,需要先排除碳酸根离子和氢氧根离子的干扰,所以加入过量的稀HNO3的目的是:完全除去NaOH、Na2CO3,以免干扰检验CaCl2;
(4)现象c:①若无白色沉淀,白色固体中不含氯离子,所以干燥剂成分为CaO和NaOH;
②若有白色沉淀,白色固体中含氯离子,干燥剂成分为CaO、CaCl2或NaOH、CaCl2;
(5)稀HNO3溶液不能用稀HCl溶液替代,否则会引入氯离子,对氯离子的检验造成干扰。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案【题目】实验小组的同学称取30g某纯碱样品,平均分成六份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后进行称量(如图所示),得到数据如表:

第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
加入样品 的质量/g | 5 | 5 | 5 | 5 | 5 | 5 |
电子天平 的示数/g | 163.9 | 167.8 | 171.7 | 175.6 | 180.6 | 185.6 |
请计算:
(1)第六次加入样品后,总共生成的二氧化碳质量是_____g。
(2)纯碱样品中碳酸钠的质量分数。_____。
【题目】学完酸碱盐之后,小明头脑里一直有疑惑,为什么老师说金属活动顺序表中钾、钙、钠很活泼,却又不能把它后面金属从盐溶液中置换出来呢?带着疑问小明走进了实验室。
(查阅资料)钠是一种活泼金属,常温下能与氧气、水等物质发生反应。钠与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑。
(实验探究)小明先取一定量的硫酸铜溶液于烧杯中,再取一小块钠投入硫酸铜溶液中,反应剧热,充分反应后过滤,得到滤液和蓝色滤渣,根据已学知识可推断蓝色滤渣为并对滤液的成分进行探究。
(猜想与假设)猜想一:Na2SO4;猜想二:Na2SO4和NaOH;猜想三_____。猜想四:Na2SO4、CuSO4和NaOH
小明认为猜想_____不合理,理由是_____(用化学方程式表示)。
(查阅资料)Na2SO4溶液呈中性
(实验与验证)
实验 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量滤液于试管中,仔细观察现象 | 溶液为无色 | 猜想_____不成立 |
实验二 | 向实验一所取滤液中滴入酚酞溶液 | _____ | 猜想一不成立 |
(拓展延伸)金属活动性顺序表中钠及前面的金属确实_____(填“能”或“不能”)把位于后面的金属从它们盐溶液里置换出来。
(继续探究)小明将4.6g钠投入到含HCl 3.65g的稀盐酸中,反应更加剧热,这是因为钠的性质很活泼,很容易失去最外层的一个电子而形成_____。请计算该过程中产生H2的质量_____。