题目内容
【题目】如图所示进行有关碳及其氧化物的性质实验,回答有关问题:
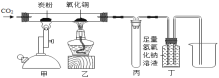
(1)甲处发生反应的化学方程式是_____,该反应是_____(填“吸热”或“放热”)反应。
(2)乙处可观察到的实验现象:_____。
(3)丙处试管的作用是_____。
(4)该装置是否需要添加尾气处理装置并说明理由:_____。
【答案】C+CO2![]() 2CO 吸热 黑色粉末逐渐变成光亮的红色 防止丁中的液体倒流入玻璃管使玻璃管炸裂 不需要,因为未反应的CO进入丁装置中,不会扩散到空气中
2CO 吸热 黑色粉末逐渐变成光亮的红色 防止丁中的液体倒流入玻璃管使玻璃管炸裂 不需要,因为未反应的CO进入丁装置中,不会扩散到空气中
【解析】
(1)二氧化碳与碳在高温的条件下反应生成一氧化碳,反应的方程式为:C+CO2![]() 2CO 。该反应需要加强热,故是吸热反应。
2CO 。该反应需要加强热,故是吸热反应。
(2)乙处氧化铜与一氧化碳在加热的条件下反应生成铜和二氧化碳,故现象为黑色粉末逐渐变红。
(3)丙处放一空试管是为了防止水倒流引起试管炸裂。
(4)没有反应的一氧化碳被丁装置收集,故不需要加装尾气处理装置。

练习册系列答案
相关题目
【题目】图表法是一种常用的数据处理方法。下表记录了氢氧化钠、碳酸钠在水和酒精中的溶解度,下列说法正确的是( )
氢氧化钠 | 碳酸钠 | |||
20℃ | 40℃ | 20℃ | 40℃ | |
水 | 109g | 129g | 21.8g | 49g |
酒精 | 17.3g | 40g | 不溶 | 不溶 |

A. 如图表示碳酸钠的溶解度曲线
B. 氢氧化钠和碳酸钠在水中都是易溶物质
C. 40℃时若将50g氢氧化钠分别投入到100g水和100g酒精中,均能形成饱和溶液
D. 20℃时将二氧化碳分别通入氢氧化钠的水溶液和酒精溶液中,均无明显现象