题目内容
【题目】在“粗盐中难溶性杂质的去除”的实验课上,同学们制得了“白色的盐”,小刚很高兴,并大声地说:“我制得了纯净的NaCl。”老师否定了他的说法,并解释说:“同学们制得的固体中除了含有NaCl外,还含有MgCl2、CaCl2、Na2SO4等可溶性杂质。”于是,同学们为了得到更纯的NaCl,设计了如下的实验方案:
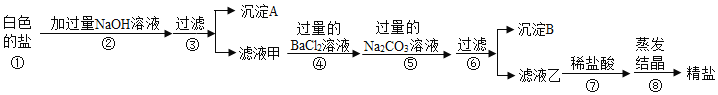
请回答下列问题:
(1)沉淀A的化学式是_____
(2)若将步骤④和⑤顺序颠倒会引发的后果是_____。
(3)沉淀B中除了含有CaCO3以外还含有_____。(填化学式)
(4)滤液乙中含有的阴离子是_____。(填离子符号)
【答案】Mg(OH)2 获得的精盐中含有氯化钡 BaSO4、BaCO3 Cl﹣、SO42﹣、CO32﹣
【解析】
根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子,进行分析解答。
(1)根据过量的氢氧化钠溶液与氯化镁溶液反应生成氢氧化镁沉淀和氯化钠,则沉淀A是氢氧化镁,其化学式为:Mg(OH)2;
(2)若将步骤④和⑤顺序颠倒,无法除去过量的氯化钡溶液,会引发的后果是获得的精盐中含有氯化钡;
(3)沉淀B中除了含有CaCO3以外,还含有硫酸钡与氯化钡溶液反应生成的硫酸钡沉淀、碳酸钠与过量的氯化钡反应生成的碳酸钡沉淀;
(4)滤液乙是氯化钠和过量的氢氧化钠、碳酸钠的混合溶液,含有的阴离子是氯离子、氢氧根离子、碳酸根离子,其离子符号分别是Cl﹣、SO42﹣、CO32﹣。

练习册系列答案
相关题目