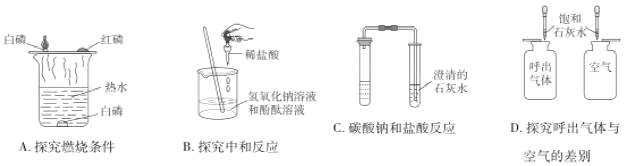
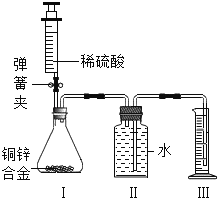
题目内容
【题目】KCl 和 KNO3 在不同温度下的溶解度数据如表所示,下列说法中正确的是( )
温度/℃ | 20 | 40 | 60 | |
溶解度/g | KCl | 33 | 38 | 45 |
KNO3 | 31 | 64 | 110 |
A. KNO3 的溶解度大于 KCl
B. 60℃时,110g KNO3 完全溶解最少需要 100g 水
C. 20℃时,KCl 饱和溶液的溶质质量分数是 33%
D. 随着温度的升高,某不饱和 KCl 溶液会变饱和
【答案】B
【解析】
A、没有确定温度,不能比较两种物质的溶解度,故A错误;
B、60℃时,硝酸钾的溶解度为110g,根据溶解度概念可知,60℃时,110g KNO3完全溶解最少需要 100g 水,故B正确;
C、一定温度下饱和溶液的溶质分数=![]() ,20℃时,KCl 的溶解度为33g,则KCl 饱和溶液的溶质质量分数=
,20℃时,KCl 的溶解度为33g,则KCl 饱和溶液的溶质质量分数=![]() ,故C错误;
,故C错误;
D、氯化钾的溶解度随着温度的升高而增大,随着温度的升高,某不饱和 KCl 溶液,溶解度会增大,溶液仍为不饱和溶液,故D错误。故选B。

【题目】在探究氢氧化钙与稀盐酸中和反应实验时,忘记了滴加酚酞溶液,无法判断反应进行到何种程度,同学们决定对反应后溶液中溶质的成分进行探究。
请写出该反应的化学方程式。_____
(提出问题)反应后溶液中的溶质是什么?
(做出猜想)猜想一:CaCl2 和 Ca(OH)2 猜想二:CaCl2 和 HCl猜想三:_____
(设计方案)
实验操作 | 实验现象 | 实验结论 |
①取少量反应后的溶液于试管中,滴加酚酞试液 | _____。 | 猜想一不正确 |
②另取少量反应后的溶液于试管中,加入_____。 | _____。 | 猜想二不正确 |
(拓展与应用)将稀盐酸逐滴匀速加入一定量的稀氢氧化钙溶液中,用数字化仪器对反应过程中溶液的温度、pH 进行实时测定,得到的曲线如图 1、图2所示。
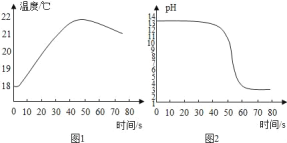
由图 1、图2知,稀盐酸与稀氢氧化钙溶液已发生中和反应的判断依据是_____。