题目内容
【题目】如图是初中化学的一些基本实验,请回答相关问题:
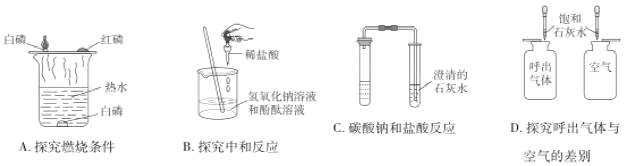
(1)A实验热水中的白磷并不燃烧,原因是_____。
(2)B实验中证明酸碱恰好中和的现象是_____。
(3)C实验中澄清的石灰水刚开始没有变浑浊,一段时间后开始变浑浊,原因是_____。(答一点即可)
(4)D实验过程中,除待测的两瓶气体体积相同外,还需控制_____相同,所观察到的现象是_____。
【答案】白磷没有与氧气接触 溶液颜色由红色变为无色 盐酸挥发出来的氯化氢气体先与氢氧化钙发生了反应 滴加饱和石灰水的量 盛有呼出气体的集气瓶内的澄清石灰水变浑浊
【解析】
(1)热水中的白磷,虽然温度达到了白磷的着火点,但是没有与氧气接触,所以并不燃烧,故填白磷没有与氧气接触。
(2)由于氢氧化钠属于碱,其溶液显碱性,则氢氧化钠溶液中滴加酚酞溶液,溶液变红色,此时溶液的pH>7,盐酸显酸性,当滴加盐酸溶液时盐酸和氢氧化钠发生反应,当两者恰好完全反应时,溶液呈中性,溶液颜色由红色变为无色,故填溶液颜色由红色变为无色。
(3)盐酸具有挥发性,挥发出来的氯化氢气体能与氢氧化钙反应生成氯化钙和水,碳酸钠与盐酸反应生成的二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,所以C实验中澄清的石灰水刚开始没有变浑浊,一段时间后开始变浑浊,原因是盐酸挥发出来的氯化氢气体先与氢氧化钙发生了反应,故填盐酸挥发出来的氯化氢气体先与氢氧化钙发生了反应。
(4)探究呼出气体和空气中二氧化碳的含量高低,滴加的饱和石灰水量也要相同,故填滴加饱和石灰水的量;
二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,会观察到盛有呼出气体的集气瓶内的澄清石灰水变浑浊,说明其中二氧化碳的浓度较大,故填盛有呼出气体的集气瓶内的澄清石灰水变浑浊。

【题目】KCl 和 KNO3 在不同温度下的溶解度数据如表所示,下列说法中正确的是( )
温度/℃ | 20 | 40 | 60 | |
溶解度/g | KCl | 33 | 38 | 45 |
KNO3 | 31 | 64 | 110 |
A. KNO3 的溶解度大于 KCl
B. 60℃时,110g KNO3 完全溶解最少需要 100g 水
C. 20℃时,KCl 饱和溶液的溶质质量分数是 33%
D. 随着温度的升高,某不饱和 KCl 溶液会变饱和