题目内容
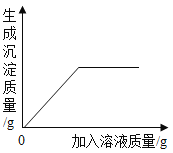
【题目】在100mL稀盐酸中加入混合均匀的NaHCO3和KHCO3固体粉末,充分反应后使气体全部逸出。下图是加入粉末的质量与产生CO2(该状况下,气体的密度为1.964g/L)体积的关系。请计算:
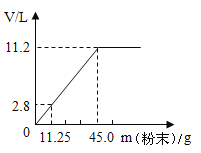
(1)该盐酸中HCl的质量多少。
(2)若该盐酸为120mL时,加入粉末为60g,求产生CO2的体积多少。
(3)若粉末的质量为xg,该盐酸的体积为160mL,产生的CO2体积为y L。试写出粉末质量x(g)与产生CO2体积y(L)之间的关系。
【答案】(1)18.25 (2)13.44 (3)x≤72 ![]() x>72 y=17.92 L
x>72 y=17.92 L
【解析】
(1)由图像可得,盐酸完全反应时产生的二氧化碳质量:![]() ,设参加反应的HCl的质量为
,设参加反应的HCl的质量为![]() 。
。
碳酸氢钠或碳酸氢钾与稀盐酸反应时,反应的化学方程式分别为为:![]() ,
,![]() ,根据化学方程式则有:
,根据化学方程式则有:

![]() ,解得
,解得![]() 。
。
答:该盐酸中HCl的质量为18.25g。
(2)由(1)中生成气体的质量可以计算出此时产生二氧化碳的体积,因为![]() ,盐酸可以全部参加反应,粉末过量,所以生成二氧化碳气体的体积为:
,盐酸可以全部参加反应,粉末过量,所以生成二氧化碳气体的体积为:![]() 。
。
答:产生CO2的体积为13.44L。
(3)![]() ,若
,若![]() ,盐酸有剩余,按照固体的质量计算,则
,盐酸有剩余,按照固体的质量计算,则![]() ;若
;若![]() ,则盐酸全部参加反应,产生的CO2体积为
,则盐酸全部参加反应,产生的CO2体积为![]() 。
。
答:若![]() ,则
,则![]() ;若
;若![]() ,
,![]() 。
。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】密闭容器中有氧气、X、水和二氧化碳4种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示。下列说法正确的是( )
物质 |
| X |
|
|
反应前质量/g | 76.0 | 16.0 | 4.0 | 3.0 |
反应后质量/g | 待测 | 0 | 40.0 | 47.0 |
A.表中待测的值为5.0
B.X由碳、氢、氧三种元素组成
C.该反应中![]() 与
与![]() 的化学计量数之比为2:1
的化学计量数之比为2:1
D.反应生成的![]() 与
与![]() 的质量比为40:47
的质量比为40:47