题目内容
【题目】结合图示实验装置,回答下列问题。
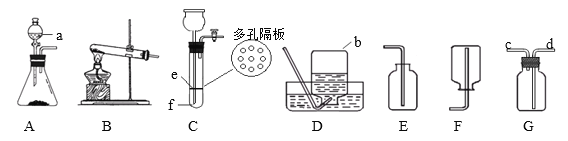
⑴图中a仪器的名称:a_______。
⑵用高锰酸钾制氧气化学方程式是___________________________。
选用的发生装置是 _______,收集装置可以是 _______(从“D”、“E”、“F”中选择)。
⑶实验室用A装置制备CO2时,反应的化学方程式是 _______________________________,若用G装置收集CO2,则气体应从__________端通入(填 “c” 或 “d” )。
⑷实验室常用来制取氢气的实验药品选用_____________________,其反应原理的基本反应类型是__________。使用C装置制取氢气的优点是__________________,则锌粒应放在 _____处(填“e”或“f”)。
【答案】 分液漏斗 2KMnO4![]() K2MnO4+MnO2+O2↑ B D或E CaCO3+2HCl=CaCl2+CO2↑+H2O d 锌和稀盐酸(或稀硫酸) 置换 可以随时控制反应的发生和停止 e
K2MnO4+MnO2+O2↑ B D或E CaCO3+2HCl=CaCl2+CO2↑+H2O d 锌和稀盐酸(或稀硫酸) 置换 可以随时控制反应的发生和停止 e
【解析】由题意可知:⑴图中a仪器的名称:分液漏斗;⑵用高锰酸钾固体制氧气,是加热固体制取气体的方法,选用的发生装置是A,反应方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑。氧气的密度比空气的大,可以用向上排空气法收集,氧气难溶于水可以用排水法收集。收集装置可以是D或E;⑶实验室制取二氧化碳时,碳酸钙和盐酸反应生成氯化钙、二氧化碳、水,反应方程式为:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑;如用E装置收集CO2,因二氧化碳密度大于空气,故气体应从c端通入;⑷实验室常用来制取氢气的实验药品选用锌和稀盐酸(或稀硫酸),改用C装置(多孔隔板用来放块状固体)代替B装置的优点是可以随时控制反应的发生与停止。关闭弹簧夹,气体增多压强增大,试管内液面下降,下降到隔板下方后,固体和液体分离,反应停止;打开弹簧夹,气体减少,压强变小,漏斗内液面下降,试管内液面上升,当固体也液体接触时,反应开始。则锌粒应放在隔板上,即e处。
K2MnO4+MnO2+O2↑。氧气的密度比空气的大,可以用向上排空气法收集,氧气难溶于水可以用排水法收集。收集装置可以是D或E;⑶实验室制取二氧化碳时,碳酸钙和盐酸反应生成氯化钙、二氧化碳、水,反应方程式为:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑;如用E装置收集CO2,因二氧化碳密度大于空气,故气体应从c端通入;⑷实验室常用来制取氢气的实验药品选用锌和稀盐酸(或稀硫酸),改用C装置(多孔隔板用来放块状固体)代替B装置的优点是可以随时控制反应的发生与停止。关闭弹簧夹,气体增多压强增大,试管内液面下降,下降到隔板下方后,固体和液体分离,反应停止;打开弹簧夹,气体减少,压强变小,漏斗内液面下降,试管内液面上升,当固体也液体接触时,反应开始。则锌粒应放在隔板上,即e处。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案