题目内容
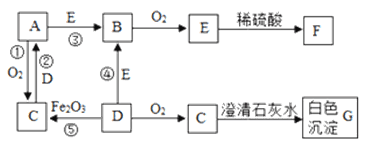
【题目】(4分)济宁是山东省重要的煤炭能源基地,然而矿区废水中Fe2+、Cu2+、Zn2+等严重影响着当地水质。某污水处理厂采用下图工艺(见下图)净化这种酸性废水并回收Fe2+、Cu2+、Zn2+三种离子。请读识流程图并回答:

(1)矿区废水经氧化池后再进入沉淀池Ⅰ,目的是____________________________________;
(2)利用氢氧化钠调节沉淀池Ⅰ、沉淀池Ⅱ和沉淀池Ⅲ的pH,目的是_____________________;
(3)出水前,中和池中加入硫酸的作用___________________;
(4)若矿区废水中主要含有硫酸盐,请写出沉淀池Ⅲ中发生反应的化学方程式__________________。
【答案】(1)将Fe2+氧化为Fe3+
(2)将离子分别沉淀
(3)中和碱性废水,防止污染环境
(4)![]()
【解析】
试题分析:(1)矿区废水中所含的Fe2+在沉淀池Ⅰ中形成了氢氧化铁沉淀。所以废水经氧化池后再进入沉淀池Ⅰ,目的是为了将Fe2+氧化为Fe3+;
(2)根据图示可知:在不同的PH环境下,分别得到了铁铜锌三种离子的沉淀,所以利用氢氧化钠调节沉淀池的pH,目的是将离子分别沉淀;
(3)因为在中和池前得到的废水为碱性,如直接出水则会造成环境污染。所以出水前,中和池中加入硫酸的作用中和碱性废水,防止污染环境;
(4)若矿区废水中主要含有硫酸盐,则在沉淀池Ⅲ中含硫酸锌。所以沉淀池Ⅲ中发生反应的化学方程式为:![]() 。
。

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目