题目内容
【题目】小明同学为探究二氧化碳的性质,设计了下列实验。
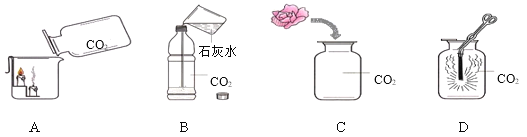
(1)装置A中的实验现象是_____;说明CO2具有的性质是_____。
(2)装置B中倒入适量澄清的石灰水后,迅速拧紧软塑料瓶的瓶盖并振荡,实验现象是_____。
(3)取一朵用石蕊溶液染成紫色的干燥小花,将小花的一半用水喷湿,放入装置C中,可观察到的实验现象是_____,发生的反应方程式为_____。
(4)仅由上述实验(3)能否得出二氧化碳与水反应的结论(填“能”或“否”)_____。
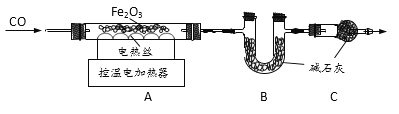
(5)小明在查阅资料时发现镁条能在二氧化碳中燃烧,他在装置D中进行实验,发现镁条剧烈燃烧,发出白光,放热,产生一种白色固体和一种黑色固体,该反应中生成的白色固体是_____,这个实验使你对燃烧条件产生的新认识是_____。
【答案】蜡烛从低到高依次熄灭(或下层蜡烛先熄灭,上层蜡烛后熄灭) 一般情况下CO2不能燃烧,也不支持燃烧;相同条件下,密度比空气大 瓶子变瘪,澄清的石灰水变浑浊 小花干燥的一半无变化,湿润的一半由紫色变为红色 CO2+H2O=H2CO3 能 MgO 燃烧不一定有氧气参加
【解析】
(1)装置A中的实验现象是蜡烛由低到高依次熄灭.故填:蜡烛由低到高依次熄灭.
该实验现象说明CO2具有的性质是一般情况下CO2不能燃烧,不支持燃烧,相同条件下,密度比空气大.故填:一般情况下CO2不能燃烧,不支持燃烧,相同条件下,密度比空气大.
(2)实验现象是瓶子变瘪,澄清的石灰水变浑浊.故填:瓶子变瘪,澄清的石灰水变浑浊.
(3)观察到的实验现象是小花干燥的一半无变化,湿润的一半变为红色.故填:小花干燥的一半无变化,湿润的一半变为红色.用水润湿的一半变红是由于二氧化碳与水反应生成了碳酸,碳酸显酸性,使石蕊变红,该反应的方程式为:CO2+H2O=H2CO3
(4)显酸性的物质能使石蕊试液变红色,根据控制变量法,此现象说明CO2能与水反应生成酸性物质.
(5)镁和二氧化碳反应能生成氧化镁和碳,该反应中没有氧气参加.故填:MgO;燃烧不一定有氧气参加.

 阅读快车系列答案
阅读快车系列答案