题目内容
【题目】向一定量的硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉质量关系如图,请回答下列问题。
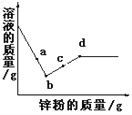
(1)a点时溶液中有哪些溶质?___________
(2)b~d段发生反应的化学方程式。__________________
(3)充分反应后发现得到固体质量增加的原因是什么? ________________
【答案】 硝酸银,硝酸铜和硝酸锌(填化学式亦可) Zn+Cu(NO3)2=Zn(NO3)2+Cu 锌与硝酸银反应使固体质量增加,与硝酸铜反应时使固体质量减少,所以固体质量可能增加(合理即可)。
【解析】(1)锌和硝酸银、硝酸铜反应的化学方程式及其反应物、生成物之间的质量关系为:
Zn+2AgNO3=Zn(NO3)2+2Ag,Zn+Cu(NO3)2=Zn(NO3)2+Cu,
65 216 65 64
由以上质量关系可知,锌和硝酸银反应时,溶液质量减小,和硝酸铜反应时,溶液质量增大,从反应开始至b点时是锌和硝酸银反应,a点时溶液中含有溶质是没有反应的硝酸银和没有反应的硝酸铜;(2)b-d段之间溶液的质量增大,是锌和硝酸铜反应生成硝酸锌和铜,发生反应的化学方程式为:Zn+Cu(NO3)2=Zn(NO3)2+Cu;(3)锌与硝酸银反应使固体质量增加,与硝酸铜反应时使固体质量减少,所以固体质量可能增加(合理即可)。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
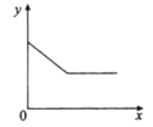
【题目】常温下,往盛有一定量液体M的烧杯中逐渐加入固体N并充分搅拌。下图中横坐标x表示固体N的质量,纵坐标y表示烧杯中的某物理量(见下表)。下列实验与图象对应关系合理的是
M | N | Y | |
A | 水 | 氧化钙 | 溶液的温度 |
B | 澄清石灰水 | 碳酸钠 | 溶液的质量 |
C | 饱和氯化钠溶液 | 氯化钠 | 溶液的溶质质量分数 |
D | 硝酸银溶液 | 铜粉 | 溶液的质量 |
A. A B. B C. C D. D