题目内容
【题目】味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于水,与AgNO3不反应),另外还含有NaCl(其他成分不考虑)。某兴趣小组配制味精溶液并测定NaCl质量分数,请回答下列问题:
(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是_____(填字母)。
A 10mL B 50mL C 100mL
(2)如图是配制过程,正确的操作顺序为_____(填序号)。
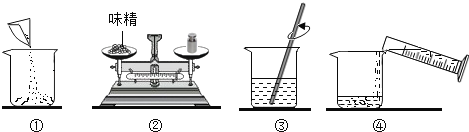
(3)为测定味精中NaCl的质量分数,进行如下实验:向所配制的50g溶液中加入AgNO3溶液充分反应后,过滤、洗涤、干燥、称量沉淀并计算。(提示:NaCl+AgNO3=NaNO3+AgCl↓)
检验过滤所得沉淀已洗涤干净的操作方法是_____。
(4)计算后发现NaCl的质量分数偏低,则可能的原因是_____(填字母)。
A 配溶液时仰视量水 B 过滤时待滤液面高于滤纸边缘 C AgNO3溶液量不足
【答案】B ②①④③ 取刚流下的洗涤液,滴加AgNO3溶液,无白色沉淀生成 B、C
【解析】
(1)配制50g溶液需要水的体积为45mL,所以量取蒸馏水的量筒规格是50mL,故填B。
(2)配制溶液的步骤是先用托盘天平称取所需的固体药品,然后将称取好的固体药品倒入烧杯中,再将量取好的溶剂倒入放有固体溶质的烧杯中,最后搅拌溶解,故填②①④③。
(3)检验过滤所得沉淀已洗涤干净的操作方法是取刚流下的洗涤液,滴加AgNO3溶液,无白色沉淀生成,故填取刚流下的洗涤液,滴加AgNO3溶液,无白色沉淀生成。
(4)A 题目中是计算味精药品中氯化钠的质量分数,配制溶液时,加水的多少不影响氯化钠的质量,选项正确;
B 过滤时待滤液面高于滤纸边缘,待滤液中的氯化银沉淀会随液体沿滤纸与漏斗内壁之间的缝隙流下,造成滤渣中的氯化银固体质量减少,计算出的氯化钠质量也偏小,选项错误;
C 加入AgNO3溶液量不足,溶液中有氯化钠剩余,求得的氯化钠质量分数偏小,选项错误,故填BC。

【题目】四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如图所示,则有关说法中不正确的( )
甲 | 乙 | 丙 | 丁 | |
反应前 | 17% | 10% | 25% | 48% |
反应后 | 19% | 10% | 41% | 30% |
A. 该反应可能是过氧化氢的分解反应
B. 乙可能是这个反应的催化剂
C. 丁一定是化合物
D. 参加反应的丁的质量一定等于生成甲和丙的质量之和