题目内容
学习化学一定要正确使用化学语言,按要求完成下列各题.(1)写出符合下列要求的化学符号或化学符号所表示的含义:
①两个氦原子
③二氧化硫中硫元素显+4价
(2)写出符合下列要求的物质的化学式或物质名称:
①含氧量最高的氧化物
③地壳中含量最多的非金属元素和最多的金属元素和空气中含量最多的元素所形成的化合物的化学式是
分析:原子用元素符号来表示.
化学符号前面的数字表示粒子的个数.
化学式或原子团中元素符号右下角的数字表示分子或原子团中原子的个数.
元素符号正上方的数字表示元素的化合价.
化学符号前面的数字表示粒子的个数.
化学式或原子团中元素符号右下角的数字表示分子或原子团中原子的个数.
元素符号正上方的数字表示元素的化合价.
解答:解:(1)①氦原子用氦的元素符号He来表示,化学符号前面的数字表示粒子的个数,因此2个氦原子表示为2He.
②化学式或原子团中元素符号右下角的数字表示分子或原子团中原子的个数,因此CO3表示1个碳酸根含有1个碳原子和3个氧原子;化学符号前面的数字表示粒子的个数,因此3CO3表示3个碳酸根.
③元素符号正上方的数字表示元素的化合价,因此二氧化硫中硫元素的化合价表示为
O2.
④HgO表示1个氧化汞分子,化学符号前面的数字表示粒子的个数,因此nHgO表示n个氧化汞分子.
(2)①由含氧量最高可知:该氧化物的分子中含氧原子个数要多,含其它原子的个数要少,且其它原子的相对原子质量要小.符合这些条件的氧化物是过氧化氢.1个过氧化氢分子含有2个氢原子和2个氧原子,化学式或原子团中元素符号右下角的数字表示分子或原子团中原子的个数,因此过氧化氢的化学式为H2O2.
②根据化学式从右往左读作“某化某”的方法,可以将NH4Cl读作氯化铵.
③地壳中含量最多的非金属元素是氧;地壳中含量最多的金属元素是铝;空气中含量最多的元素是氮.三种元素中的氮和氧可以形成硝酸根,铝与硝酸根可以形成硝酸铝,1个硝酸铝分子中含有1个铝原子和3个硝酸根,1个硝酸根含有1个氮原子和3个氧原子,化学式或原子团中元素符号右下角的数字表示分子或原子团中原子的个数,因此硝酸铝的化学式是Al(NO3)3.
故答案为:
(1)①2He;②3个碳酸根;③
O2;④n个氧化汞分子.
(2)①H2O2;②氯化铵;③Al(NO3)3.
②化学式或原子团中元素符号右下角的数字表示分子或原子团中原子的个数,因此CO3表示1个碳酸根含有1个碳原子和3个氧原子;化学符号前面的数字表示粒子的个数,因此3CO3表示3个碳酸根.
③元素符号正上方的数字表示元素的化合价,因此二氧化硫中硫元素的化合价表示为
| +4 |
| S |
④HgO表示1个氧化汞分子,化学符号前面的数字表示粒子的个数,因此nHgO表示n个氧化汞分子.
(2)①由含氧量最高可知:该氧化物的分子中含氧原子个数要多,含其它原子的个数要少,且其它原子的相对原子质量要小.符合这些条件的氧化物是过氧化氢.1个过氧化氢分子含有2个氢原子和2个氧原子,化学式或原子团中元素符号右下角的数字表示分子或原子团中原子的个数,因此过氧化氢的化学式为H2O2.
②根据化学式从右往左读作“某化某”的方法,可以将NH4Cl读作氯化铵.
③地壳中含量最多的非金属元素是氧;地壳中含量最多的金属元素是铝;空气中含量最多的元素是氮.三种元素中的氮和氧可以形成硝酸根,铝与硝酸根可以形成硝酸铝,1个硝酸铝分子中含有1个铝原子和3个硝酸根,1个硝酸根含有1个氮原子和3个氧原子,化学式或原子团中元素符号右下角的数字表示分子或原子团中原子的个数,因此硝酸铝的化学式是Al(NO3)3.
故答案为:
(1)①2He;②3个碳酸根;③
| +4 |
| S |
(2)①H2O2;②氯化铵;③Al(NO3)3.
点评:本题主要考查元素符号和化学式的书写、化合价的标注、化学式的读法及多个粒子的表示,难度稍大.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
某校外化学兴趣小组同学学习化学积极性高,平时喜欢收集化学用品,建立了他们自己的实验室,其实验室中部分仪器如图.
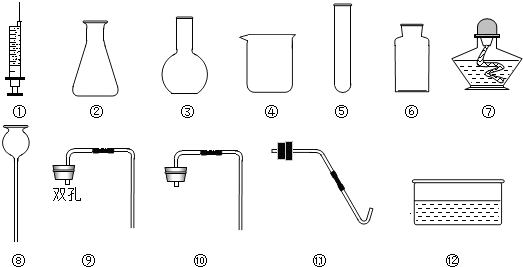
(1)①指出下列仪器名称:⑤ ;⑦ ;
②该小组同学经过认真讨论,一致认为从二氧化碳制取原理和溶解性角度考虑,在设计制取和收集二氧化碳的装置时,一定不会选用上述仪器中的 .(填序号)
③该小组小霞、小红和小华三位同学利用上述仪器各自设计出一种制取和收集二氧化碳的装置,用到的仪器如下:小霞:④⑥⑩小红:①②⑥⑨小华:②⑥⑧⑩
该组同学经过积极讨论和实验验证,大家一致认为小霞和小华设计的实验装置不能达到实验目的,那么请你也参与他们的讨论:
A.小霞同学实验不能达到目的原因是 .
小红同学要想顺利完成实验,有两种改进方法:即仪器①用仪器 替代,或用仪器 替代仪器⑨.
B.小红同学设计的装置还可以用来制取氧气,她采用的实验室制气原理为(用化学方程式表示) .
(2)小红同学为探究二氧化碳与水反应的生成物,做了如下实验:
向盛有石蕊试液的试管中通入二氧化碳,观察到紫色石蕊试液变成了红色.为了探究是什么物质使紫色石蕊变红了,小红同学作了大胆猜想,并用石蕊溶液染成紫色的干燥的小花设计了下列四个实验方案来验证自己的猜想(如图).
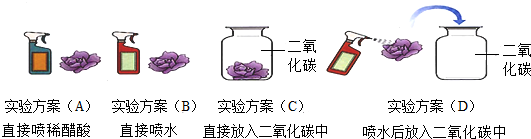
①请和小红同学一起完成下表.
②小红同学做了一个对比实验来确定CO2与水反应生成具有酸性的物质,此对比实验方案是 (填上图中的实验方案序号).

(1)①指出下列仪器名称:⑤
②该小组同学经过认真讨论,一致认为从二氧化碳制取原理和溶解性角度考虑,在设计制取和收集二氧化碳的装置时,一定不会选用上述仪器中的
③该小组小霞、小红和小华三位同学利用上述仪器各自设计出一种制取和收集二氧化碳的装置,用到的仪器如下:小霞:④⑥⑩小红:①②⑥⑨小华:②⑥⑧⑩
该组同学经过积极讨论和实验验证,大家一致认为小霞和小华设计的实验装置不能达到实验目的,那么请你也参与他们的讨论:
A.小霞同学实验不能达到目的原因是
小红同学要想顺利完成实验,有两种改进方法:即仪器①用仪器
B.小红同学设计的装置还可以用来制取氧气,她采用的实验室制气原理为(用化学方程式表示)
(2)小红同学为探究二氧化碳与水反应的生成物,做了如下实验:
向盛有石蕊试液的试管中通入二氧化碳,观察到紫色石蕊试液变成了红色.为了探究是什么物质使紫色石蕊变红了,小红同学作了大胆猜想,并用石蕊溶液染成紫色的干燥的小花设计了下列四个实验方案来验证自己的猜想(如图).

①请和小红同学一起完成下表.
| 猜想 | 实验方案 | 实验现象 | 结论 |
| 可能是CO2 使石蕊变红 | C | 紫色小花不变色 | |
| B | 紫色小花不变色 | 猜想错误 | |
| 可能是CO2 和水发生反应的生成物使石蕊变红 | 猜想正确 |