题目内容
【题目】在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金属,其发生反应的质量关系如图所示,读识如图并判断,下面推理合理的是( )
①反应速率:Mg>Fe>Zn ②反应生成氢气质量:Mg=Fe=Zn
③反应后溶液质量:Mg=Fe=Zn ④反应后溶液溶质质量分数:Mg<Fe<Zn.
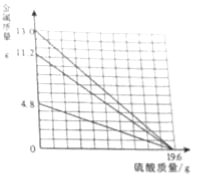
A.①② B.③④ C.①③ D.②④
【答案】D
【解析】镁、锌、铁和硫酸反应的化学方程式为:
Mg+H2SO4=MgSO4+H2↑
24 98 2
4.8g 0.4g
反应后溶质为:19.6g+4.8g﹣0.4g=24g
溶质质量分数为:![]() ×100%
×100%
Zn+H2SO4=ZnSO4+H2↑
65 98 2
13g 0.4g
反应后溶质为:19.6+13g﹣0.4g=32.2g
溶质质量分数为:![]() ×100%
×100%
Fe+H2SO4=FeSO4+H2↑
56 2
11.2g 0.4g
反应后溶质为:19.6g+11.2g﹣0.4g=30.4g
溶质质量分数为:![]() ×100%
×100%
①三种金属的活动性顺序为:Mg>Zn>Fe,所以反应速率:Mg>Zn>Fe,故错误;
②依据化学方程式可知,反应生成氢气质量:Mg=Fe=Zn,故正确;
③通过推导可知,硫酸中的溶剂质量相等,反应后溶液质量:Mg<Fe<Zn,故错误;
④通过计算比较可知,反应后溶液溶质质量分数:Mg<Fe<Zn,故正确.
故选:D.

 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案【题目】下列化学方程式及其反应类型都正确的是
选项 | 化学方程式 | 反应类型 |
A | Mg+O2 | 化合反应 |
B | H2O2 | 分解反应 |
C | Fe+H2SO4=FeSO4+H2↑ | 置换反应 |
D | 2KNO3+Ba(OH)2=Ba(NO3)2+2KOH | 复分解反应 |
A.AB.BC.CD.D
【题目】某化学兴趣小组称取4.0 g石灰石样品,把40 g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入10 g | 3.0 g |
第二次加入10 g | 2.0 g |
第三次加入10 g | 1.0 g |
第四次加入10 g | 0.6 g |
请计算:
(1)4.0 g石灰石样品中碳酸钙的质量是_____g。
(2)求稀盐酸的溶质质量分数。