题目内容
(8分)随着人们对酒驾危害认识的加深,司法机关对于酒驾、醉驾的处罚将日趋加重。醉酒的原因是酒中含有的乙醇对人的神经系统有刺激作用。交警对呼气酒精检验的原理是:橙色的K2Cr2O7酸性溶液遇乙醇会迅速变成蓝绿色。
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸。小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性。在加热条件下,可以把氧化铜还原为单质铜。
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性。
【提出猜想】猜想1:只有乙醇
猜想2:只有乙酸
猜想3:
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白酒于试管中,滴入几滴橙色的K2Cr2O7酸性溶液 | | 猜想3成立 |
| ② | |
【提出猜想】猜想3:既有乙醇,又有乙酸(1分)
【实验探究】
【实验反思】不能(1分) 乙酸也能使铜丝表面由黑色变为红色(2分)(合理即可)实验操作 实验现象 实验结论 溶液呈蓝绿色(1分) ②取少量白酒于试管中,滴入几滴紫色石蕊试液。(或取少量碳酸钠溶液于试管中,滴入适量白酒)[其他合理答案同样给分](2分) 溶液显红色
(有气泡放出)(1分)
解析试题分析:【提出猜想】根据题目描述可知,如白酒中的乙醇没有转化,则其成分只有乙醇;如白酒中的乙醇完全转化,则其成分只有乙酸;如白酒中的乙醇部分转化,则其成分为乙醇和乙酸的混合物;
【实验探究】因实验结论为:猜想3成立。即白酒中即有乙醇,又存在乙酸;所以操作①的现象应为:溶液呈蓝绿色;操作②可利用乙酸的酸性来检验乙酸是否存在。具体操作可为:取少量白酒于试管中,滴入几滴紫色石蕊试液。实验现象为溶液显红色。即可说明溶液中有呈酸性的乙酸存在。
【实验反思】乙酸呈酸性,可与氧化铜反应生成可溶于水的硫酸铜而除去黑色物质,使铜丝表面由黑色变为红色。所以不能将操作①改为“将加热后的表面有黑色氧化铜的铜丝插入盛有白酒的试管中”。
考点:科学探究

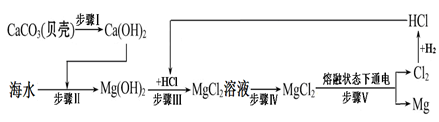
某实验小组利用废硫酸液制备K2SO4并研究CaSO4?2H2O加热分解的产物.
(一)K2SO4的制备
(1)将CaCO3研成粉末的目的是 .
(2)上述流程中可循环使用的物质有CO2和 (填写化学式).
(3)反应Ⅲ中相关物质的溶解度如下表.你认为反应Ⅲ在常温下能实现的原因是 .
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是 ;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入 (选填序号,下同),振荡、静置,再向上层清液中滴加 ,观察现象即可判断.
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液
(二)研究CaSO4?2H2O加热分解的产物.
(5)分离所得的CaSO4?2H2O含有CaCO3,可用盐酸除去,该的化学反应方程式 .
(6)为了测定CaSO4?2H2O和CaCO3的质量比x:y,实验小组利用如图所示的装置(夹持仪器省略)进行实验.
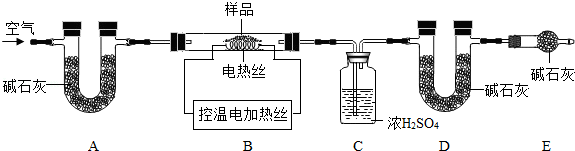
①实验前首先要 ,再装入样品.装置A的作用是 .
②已知CaSO4?2H2O在160℃生成CaSO4,1350℃时CaSO4开始分解;CaCO3在900℃时分解完全.现控制B装置温度900℃进行实验并采集了如下数据:
a.反应前玻璃管与样品的质量m1g b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g
某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将 (填“偏大”、“偏小”或“无影响”).你认为还可选用上述的 (选填序号)两个数据组合也可求出x:y的值.
(7)CaSO4?2H2O受热会逐步失去结晶水.取纯净CaSO4?2H2O固体3.44g,放在(5)的实验装置B中进行加热,测定固体质量随温度的变化情况如图所示.①G点固体的化学式是 .

②将T2~1400℃温度段加热固体所产生的气体通入酸性KMnO4溶液中,溶液褪色,则H~I段发生反应的化学方程式为 .
“五·一”小长假后,小刚和小敏带着快乐的心情返回学校。当他们来到实验室时,意外地发现实验桌上有一瓶敞口放置的氢氧化钠固体,由此,激发了他们的探究欲望。
【提出问题】这瓶氢氧化钠固体是否变质?
氢氧化钠露置在空气中变质的原因是 (用化学方程式表示)。
【提出猜想】猜想一:没有变质;
猜想二:部分变质;
猜想三:全部变质。
【实验探究】小刚和小强设计了如下实验方案:
小刚:取少量样品加适量蒸馏水配成溶液后,滴入几滴酚酞溶液,若观察到溶液变红色,证明该瓶氢氧化钠固体没有变质。
小敏认为小刚的结论是错误的,理由是 。
于是小敏进行了如下实验:
(1)上述实验操作④的名称 ,其中玻璃棒的作用 。
(2)步骤③中加过量氯化钙溶液的目的是 。
(3)步骤⑤中,小敏用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,
他判断猜想二是正确的。对他的操作方法、测量结果及结论的评价,正确的是 。
| A.方法正确,结果正确,且结论正确 |
| B.方法正确,结果正确,结论不正确 |
| C.方法不正确,结果偏大,但结论正确 |
| D.方法不正确,结果偏小,但结论正确 |
(1)在实验室里氢氧化钠需要密封保存。药品密封保存的原因很多,请你写出浓硫酸需要
密封保存的原因 。
(2)下列物质能替代小敏实验中CaCl2溶液的是 (填序号)。
①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH) 2溶液、④Ba(OH)2 溶液。
(6分)某化学兴趣小组在做完制取二氧化碳的实验后(用石灰石和稀盐酸制取),对反应后反应器内的剩余溶液的溶质成分产生了兴趣,他们继续进行了以下实验探究。
【分析推断】根据制取二氧化碳的反应原理,可以确定剩余溶液中一定含有氯化钙。但其中是否含有氯化氢需要通过实验来证明。若剩余溶液显酸性(含有H+),说明含有氯化氢。
【查阅资料】碳酸钙不溶于水,氢氧化钙微溶于水,氯化钙溶液呈中性。
【实验过程】将剩余的溶液倒入烧杯中,微热后冷却到室温。请设计三种实验方案,用三种不同类别的物质检验烧杯中的溶液是否含有氯化氢,并根据实验过程完成下表需填写的内容。
| | 实验操作 | 实验现象 | 实验结论 |
| 方案一 | 取烧杯中溶液少许于试管中,向其中滴加2至3滴紫色石蕊试液 | | 溶液显酸性(含有H+);溶质中有氯化氢。 |
| 方案二 | | 有气泡产生 | |
| 方案三 | | |
请你参与实验室用生石灰制取氢氧化钠固体的研究。将一定量的生石灰加入一只洁净的
烧杯中,加入碳酸钠溶液,充分反应后冷却到室温,通过过滤、洗涤、干燥得到固体A和
溶液B,请回答以下问题。
【查阅资料】NaOH 、Ca(OH)2的溶解度
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| NaOH的溶解度(g/100g水) | 42 | 109 | 129 | 174 | 314 | 347 |
| Ca(OH)2的溶解度(g/100g水)[来源: | 0.18 | 0.16 | 0.14 | 0. 12 | 0.09 | 0.07 |
(1)固体A中的成分是什么?
【猜想与假设】
甲同学认为是:CaCO3 乙同学认为是:CaCO3,Ca(OH)2
乙同学猜想可能含有Ca(OH)2的理由是 (用化学方程式表示)。
【实验与探究】为了验证各自的猜想,甲、乙同学分别进行了实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 甲同学:用一支洁净的试管取少量固体A,再加入过量稀盐酸。 | 有气泡产生 | 自己的猜想 正确 |
| 乙同学:用一支洁净的试管取少量固体A,加水,充分振荡,向上层清液中滴加 。 | 上层清液由无色变为红色 | 自己的猜想 正确 |
【反思与评价】同学讨论后认为,甲同学的实验 (填“能”或“不能”)证明固体A的成分,理由是 ;
结合甲、乙两位同学的实验证明了乙同学的猜想是正确的,因此确定了固体A的成分。
(2)溶液B中溶质的成分是什么?
【猜想与假设】丙同学认为是:NaOH、Na2CO3
丁同学认为是:NaOH、Ca(OH)2
戊同学认为是:NaOH
【表达与交流】
①结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由是 ;
②同学们欲将溶液B加热浓缩,加热不久,溶液出现浑浊,只好停止加热,请解释加热时溶液出现浑浊的原因是 ;
③同学们立即变换方案,向B溶液中加入适量的 ,过滤,将滤液加热浓缩至饱和, 、过滤、洗涤、烘干得到比较纯净的氢氧化钠固体。
④取少量制取的氢氧化钠固体溶解,进行焰色反应,观察到火焰呈 色。