题目内容
【题目】初中化学几种常见物质间的转化关系如图所示。其中A是人体胃液中含有的成分,B可用于改良酸性土壤,G是铁锈的主要成分(Fe2O3·xH2O),E、F、I均为无色气体。请回答下列问题。
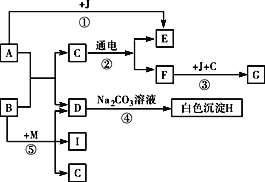
(1)写出有关物质的化学式:A _______,D_______,J_______,H________。
(2)写出有关反应的化学方程式:
反应:__________;
反应⑤:__________。
【答案】HCl CaCl2 Fe CaCO3 2H2O![]() 2H2↑+O2↑ Ca(OH)2+2NH4Cl= CaCl2+ 2H2O+2NH3↑
2H2↑+O2↑ Ca(OH)2+2NH4Cl= CaCl2+ 2H2O+2NH3↑
【解析】
由人体胃液中的主要成分是胃酸即盐酸可知A是盐酸,生活中常用熟石灰来改良酸性土壤,所以B是熟石灰,A和B反应生成水和氯化钙;又因为水通电分解生成氢气和氧气,那么C是水,D就是氯化钙,反应④就是氯化钙和碳酸钠的反应,生成氯化钠和白色难溶于水的碳酸钙沉淀,符合复分解反应发生的条件,所以白色沉淀H是碳酸钙;铁锈是由铁和空气中的氧气、水蒸汽反应得到的,所以F是氧气,J是铁,E就是氢气;又因为I也是无色气体,能和碱反应生成气体的是铵盐,I应当是氨气,又因为D是氯化钙,根据复分解反应的定义逆推可知M是氯化铵,所以反应⑤是氢氧化钙和氯化铵反应生成氯化钙、水和氨气的反应。由上分析可知
(1)A是盐酸,故填HCl;D是氯化钙,故填CaCl2;J是铁,故填Fe;H是碳酸钙,故填CaCO3;
(2)反应②是水通电分解生成氢气和氧气的反应,故填2H2O![]() 2H2↑+O2↑;反应⑤是氢氧化钙和氯化铵反应生成氯化钙、水和氨气的反应,故填Ca(OH)2+2NH4Cl= CaCl2+ 2H2O+2NH3↑。
2H2↑+O2↑;反应⑤是氢氧化钙和氯化铵反应生成氯化钙、水和氨气的反应,故填Ca(OH)2+2NH4Cl= CaCl2+ 2H2O+2NH3↑。

【题目】某同学欲探究 “双钙防蛀”牙膏、“皓清”牙膏和牙粉的主要成分。
(查阅资料)(1)牙膏和牙粉均是由摩擦剂、活性剂、香料等成分构成。
(2)常用的摩擦剂有极细颗粒的碳酸钙(CaCO3) 和水合硅酸(SiO2·nH2O)等。
(3)牙膏和牙粉中除了碳酸钙以外,其它物质均不与稀盐酸反应产生气体。
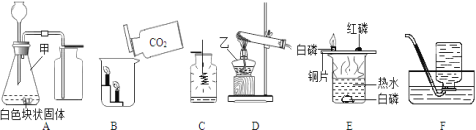
(实验一)探究“两种牙膏和牙粉中是否都含有碳酸钙?
步骤 | 实验操作 | 实验现象 |
① |
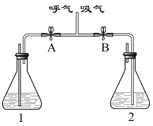
如图所示,取三只试管分别加入适量待测样品,再分别加入适量x稀溶液。x稀溶液是____________。 | A试管中无明显变化, B和C试管中有无色气体生成。 |
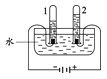
② | 将B和C试管中生成的无色气体通入__________。 | 现象Ⅱ:____________。 |
实验结论: _________________ 。碳酸钙与x稀溶液反应的化学方程式为为_________。
(实验二)比较样品中碳酸钙的含量
步骤 | 实验操作 | 实验现象 |
① |
| |
② | 打开分液漏斗注入一定量x稀溶液,然后关闭活塞。 | 有气泡产生。 |
③ | 待②反应结束后,再打开分液漏斗,注入一定量x稀溶液,然后关闭活塞。 | 无明显现象 |
④ | 称量反应后装置及药品的总质量并加以比较 | 加入“双钙防蛀”牙膏的装置及药品的总质量大于加入牙粉的装置及药品的总质量 |
实验结论:____________
(反思)若不改动原有装置和基本步骤,要测定牙粉中碳酸钙的质量分数,还应测定的数据有:__________。