题目内容
水与人类的生活、生产密切相关。
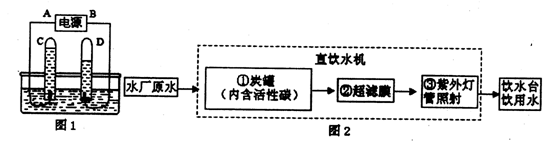
(1)如图所示,电极上可观察到的现象是 。反应的化学方程式是 。
(2)自来水生产过程中通入氯气的作用是 。
(3)高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂。
K2FeO4的摩尔质量是 。 1mol K2FeO4含有 个氧原子。高铁酸钾受热分解的化学方程式是:4K2FeO4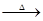 2R+4K2O+3O2↑,则R是 (填化学式)。
2R+4K2O+3O2↑,则R是 (填化学式)。
(4)对生活污水再利用是节水的重要手段。某生活污水含有碎菜叶、泥沙,可能含有氯化钠和碳酸钠可溶性物质。
Ⅰ.去掉水中的碎菜叶等较大的固体后,再对污水进行 操作可除去其中泥沙等小颗粒物质。
Ⅱ.为了检验经Ⅰ处理后的水样中是否存在氯化钠、碳酸钠,某同学设计实验流程如下: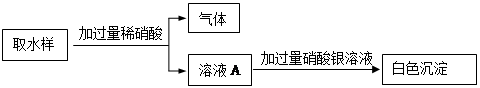
检验气体的试剂是 。溶液A中含有的溶质是 。在水样中加入稀硝酸不能改成稀硫酸,理由是 。
结论:该生活污水中含有 (写化学式)可溶性物质。
(1)产生气泡 2H2O 2H2↑+O2↑
2H2↑+O2↑
(2)消毒杀菌
(3)198g/mol 2.408×1024 Fe2O3
(4)过滤 澄清石灰水 HNO3、NaNO3、NaCl(2分)
生成的Ag2SO4干扰对NaCl的检验 NaCl、Na2CO3
解析试题分析:(1)水电解过程中有氢气和氧气放出,所以电极上观察到的现象是有气泡产生,化学方程式为2H2O 2H2↑+O2↑
2H2↑+O2↑
(2)自来水生产过程中通入氯气的作用是杀菌和消毒
(3)K2FeO4的摩尔质量是198g/mol,摩尔质量的单位为g/mol,不能忘了单位,1mol K2FeO4含有4mol的氧原子,所以含有4×6.02×1023个氧原子,根据原子守恒得到R的化学式为Fe2O3,
(4)通过过滤可以除去水中的泥沙等固体小颗粒,加稀硝酸产生的气体为二氧化碳,检验二氧化碳用澄清石灰水,溶液A中含有的溶质有HNO3,还有生成的NaNO3,还有未反应的NaCl,改成稀硫酸,会和硝酸银反应生成硫酸银沉淀,而检验氯化钠会生成氯化银沉淀,所以会干扰氯化钠的检验,根据使用现象推得污水中含有氯化钠和碳酸钠。
考点:水的电解,水的净化,溶质的判断

 阅读快车系列答案
阅读快车系列答案(3分)稀薄燃烧发动机具有高效、经济、环保等优点,和普通汽车发动机对比如下:
| 发动机类型 | 发动机混合气中汽 油与空气的质量比 | 发动机运 转时温度 | 尾气中 CO的含量 | 尾气中 NOx的含量 |
| 普通发动机 | 1:15 | 较高 | 较高 | 较高 |
| 稀薄燃烧发动机 | 1:40 | 较低 | 较低 | 较低 |
A.发动机混合气中的汽油含量低 B.发动机混合气中的空气含量低
C.发动机混合气中氧气的含量低 D.发动机混合气中氮气的含量低
⑵ 为何稀薄燃烧发动机产生的尾气中CO含量会减少? 。
⑶ 某种减少尾气中CO与NOX的方法是使用催化转换器,转换过程中发生反应的化学方程式为:CO+NOx→CO2+N2(未配平)。若x = 1.5,则化学方程式中CO2与N2的系数之比为 。
为了加快建设美好幸福新铜仁,市委、市人民政府提出建设“武陵之都,仁义之城”的目标,为铜仁发展注入了新的内涵。
(1)铜仁市水资源比较丰富,请提出防止水污染的几种措施(2条以上)。
(2)下列措施不利于我市可持续发展的是 (填字母)
| A.加大城市绿化、园林建设 | B.大力发展火力发电 |
| C.注重地方文化传承及发展 | D.发展工业与环保相结合 |