题目内容
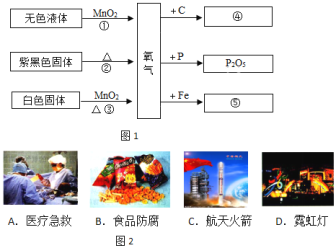
【题目】A、B、C、D都是九年级化学中的物质,它们存在如图所示的关系(反应
条件略去).
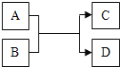
(1)该反应一定不属于分解反应和_____________反应.
(2)若A为一氧化碳,C为金属,则D为_______________
(3)若A为常见金属,C为气体单质,则B为___________
(4)若A为蓝色溶液,C为浅绿色溶液,则该反应的化学方程式为________。
【答案】化合 CO2 HCl或H2SO4 Fe+CuSO4=Cu+FeSO4
【解析】
(1)反应物和生成物都是两种,一定不是化合反应和分解反应;
(2)A是一氧化碳,C是金属,所以B就是金属氧化物,D就是二氧化碳;
(3)A为常见金属,C为气体单质,符合置换反应的定义,所以B是酸;
(4)A为蓝色溶液,C为浅绿色溶液,所以A中含有铜离子,C中含有亚铁离子,所以B就是铁,C就是铜,反应的化学方程式为: Fe+CuSO4═Cu+FeSO4。

【题目】镁条在空气中久置表面会变黑。某小组同学设计实验,探究镁条变黑的条件。
(查阅资料)①NaOH浓溶液能与二氧化碳反应,化学方程式为:
2NaOH+CO2=Na2CO3+H2O
②浓硫酸有吸水性,常用做气体的干燥剂
③常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
(猜想与假设)常温下,镁条变黑可能与O2、CO2、水蒸气有关。
(进行实验)通过控制与镁条接触的物质,利用下图装置(镁条长度为3 cm,试管容积为20 mL)分别进行下列5个实验,并持续观察20天。

编号 | 主要实验操作 | 实验现象 |
1 | 先充满用NaOH浓溶液洗涤过的空气再加入2mL浓硫酸 | 镁条始终无明显变化 |
2 | 加入2mLNaOH浓溶液 | 镁条始终无明显变化 |
3 | 先加入2mL浓硫酸 再通入约4mLCO2 | 镁条始终无明显变化 |
4 | 先加入4mL饱和Na2SO3溶液 再充满CO2 | 镁条始终无明显变化 |
5 | 先加入2mL蒸馏水 再通入约4mLCO2 | 镁条第3天开始变黑 至第20天全部变黑 |
(解释与结论)
(1)实验1和2中,NaOH浓溶液的作用是____________。
(2)实验1的目的是__________。
(3)实验3中,试管内的气体主要含有CO2、___________。
(4)得出“镁条变黑一定与CO2有关”的结论,依据的两个实验是___________(填编号)。
(5)由上述实验可推知,镁条变黑的条件是__________。
(反思与评价)
(6)在猜想与假设时,同学们认为镁条变黑与N2和稀有气体无关,其理由是__________。
(7)由质量守恒定律推测,镁条变黑后的生成物中一定含有___________元素。