题目内容
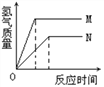
【题目】现把镁条投入盛有稀盐酸的试管中如图所示,试管外壁发烫产生氢气的速率变化情况(v)和反应进行的时间(t)的关系如图所示,则下列说法不正确的是()

A. 反应中试管外壁发烫,说明镁与稀盐酸反应是放热反应
B. 向反应后的溶液中滴入酚酞溶液,振荡显无色,说明溶液显酸性
C. ![]() 时间段反应速率变化,说明化学反应速率受温度的影响
时间段反应速率变化,说明化学反应速率受温度的影响
D. ![]() 时间段反应速率变化的主要原因是盐酸的浓度逐渐减小
时间段反应速率变化的主要原因是盐酸的浓度逐渐减小
【答案】B
【解析】
A、试管外壁发烫,说明反应放热,说法正确,故不符合题意;
B、镁和稀盐酸反应生成氯化镁和氢气,溶液显中性,滴入酚酞,溶液也显无色,说法不正确,故符合题意;
C、![]() 速率变化的主要原因是随着反应进行,反应放热,反应速率增大,选项说法正确,故不符合题意;
速率变化的主要原因是随着反应进行,反应放热,反应速率增大,选项说法正确,故不符合题意;
D、![]() 速率变化的主要原因是盐酸的浓度逐渐减小,反应速率减小,选项说法正确,故不符合题意。故选B。
速率变化的主要原因是盐酸的浓度逐渐减小,反应速率减小,选项说法正确,故不符合题意。故选B。

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案【题目】等质量的铁粉与过量的盐酸在不同的实验条件下进行反应,测定在相同时间t内产生气体体积V的数据,根据数据绘制得到图1。
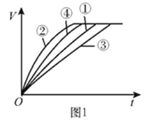
组别 | 盐酸的溶质质量分数/% | 温度/℃ |
① | 7 | 30 |
② | 10 | 50 |
③ | 7 | 20 |
④ | 10 | 30 |
(1)请写出铁粉与稀盐酸反应的化学方程式:________。
(2)通过实验①③对比,得出的结论是________;要比较盐酸的溶质质量分数对反应快慢的影响,应选择的实验组别是________。
(3)实验中产生气体“逐渐变快又变慢”的原因是________。
(进一步探究)图甲、图乙为利用数字化仪器测得的室温下足量的三种金属片分别与20 mL 10%的稀盐酸反应产生氢气的量(产生氢气的量由气体压强表示,在等温条件下,产生氢气的体积与装置内压强成正比)。
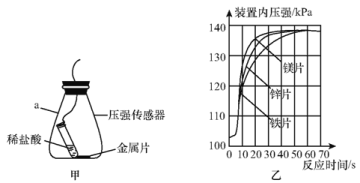

①实验中你认为还要控制的变量是________。
②根据图乙,你得出的反应物的量与生成的气体体积的关系是________。
(拓展提高)图2为测得的室温下足量的镁片与20 mL 10%的稀盐酸反应产生氢气的量与时间的关系曲线,发现实验测得的实际值比通过计算得到的理论值偏大,请分析可能的原因(至少答两点):
①________;②________。