题目内容
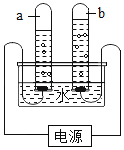
【题目】利用如图所示装置进行实验。从A或B中任选一个作答,若均作答,按A计分。
A | B |
A处观察到的现象为________,产生该现象的原因为________。 |
A处观察到的现象为_______,产生该现象的原因为________。 |
【答案】红色棉球褪色 浓盐酸挥发出氯化氢气体,遇水形成盐酸,与氢氧化钠反应 棉球由紫色变成红色 石灰石与稀盐酸反应产生二氧化碳,二氧化碳与A处水反应生成碳酸,石蕊遇碳酸变红
【解析】
(A)浓盐酸由挥发性,挥发的HCl气体与A处的氢氧化钠溶液反应生成中性的氯化钠和水,故A处红色棉球褪色,产生该现象的原因为浓盐酸挥发出氯化氢气体,遇水形成盐酸,与氢氧化钠反应。
故填:红色棉球褪色;浓盐酸挥发出氯化氢气体,遇水形成盐酸,与氢氧化钠反应;
(B) B处石灰石与稀盐酸反应产生二氧化碳,二氧化碳与A处水反应生成碳酸,石蕊遇碳酸变红。故填:棉球由紫色变成红色;石灰石与稀盐酸反应产生二氧化碳,二氧化碳与A处水反应生成碳酸,石蕊遇碳酸变红。

【题目】小明同学对所学部分化学知识归纳如下。其中不正确的是( )
A | 须辨清的物质 | B | 初中化学中常见的“三” |
干冰不是冰﹣而是固体CO2 纯碱不是碱﹣而是盐 | 三种常见还原剂CO、H2、C 三种基本粒子﹣﹣原子、分子、离子 | ||
C | 化学巨匠及其杰出贡献 | D | 符号中数字“2”的意义 |
张青莲﹣测量相对原子质量 侯德榜﹣﹣发明联合制碱法 |
2O:两个氧原子 |
A. AB. BC. CD. D
【题目】工业上常采用“双碱法”除去烟气中的![]() ,工业流程示意图如下.
,工业流程示意图如下.
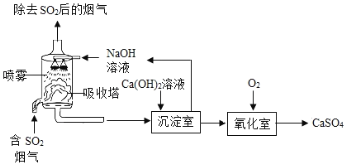
(1)吸收塔中,用NaOH溶液吸收![]() ,化学反应方程式是___.NaOH溶液喷成雾状能充分吸收SO2的原因是_____
,化学反应方程式是___.NaOH溶液喷成雾状能充分吸收SO2的原因是_____
(2)氧化室中,化学反应方程式是_______。
(3)已知部分原料的价格如表所示.
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.90 |
上述工业流程中,处理相同量的![]() ,双碱法所需的原料成本比用NaOH直接吸收更低,原因是___
,双碱法所需的原料成本比用NaOH直接吸收更低,原因是___
(4)某中学化学兴趣小组为测定工厂周围的空气中的二氧化硫含量是否符合国家标准,将![]() 周围空气通入一定含量碘(
周围空气通入一定含量碘(![]() )2.54mg的碘水中,经测定I2与二氧化硫恰好完全反应,该反应的化学方程式是
)2.54mg的碘水中,经测定I2与二氧化硫恰好完全反应,该反应的化学方程式是![]() 。通过计算说明此烟气排放后周围空气中二氧化硫的浓度级别______。
。通过计算说明此烟气排放后周围空气中二氧化硫的浓度级别______。
[资料信息:我国空气质量标准对空气中二氧化硫的浓度级别规定如下表所示(空气中二氧化硫的浓度用单位体积的空气中所含二氧化硫的质量表示)]。
浓度级别 | 标准(mg·m-3) |
一级 | 浓度≤0.15 |
二级 | 0.15<浓度≤0.50 |
三级 | 0.50<浓度≤0.70 |