题目内容
有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化.根据以上实验事实判断,以下金属活动性由强到弱的顺序是( )
| A、Y Ag Z X |
| B、Y X Z Ag |
| C、X Y Ag Z |
| D、X Ag Y Z |
考点:金属活动性顺序及其应用
专题:金属与金属材料
分析:根据①在金属活动性顺序中,排在氢前面的金属能与酸反应置换出氢气,排在后面的则不能;②活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来.可以较为容易的判断出X、Y、Z、Ag的金属的活动性顺序.
解答:解:由题中把X和Y分别放入稀硫酸中,X可以反应产生氢气,Y不反应,可知X位于氢之前,Y位于氢后;而把Y和Z放入硝酸银溶液中,过一会儿,在Y表面有银析出,Z没有变化说明Y位于银之前,Z位于银之后.就是说X、Y、Z、Ag的金属活动性顺序由强到弱应是X、(H)、Y、Ag、Z.我们据此对四个选项判断即可.
故选C.
故选C.
点评:本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行分析,难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
欲中和氯化钙溶液中少量的盐酸,在没有指示剂的条件下应选用的试剂是( )
| A、石灰石粉末 |
| B、生石灰粉末 |
| C、熟石灰粉末 |
| D、硝酸银溶液 |
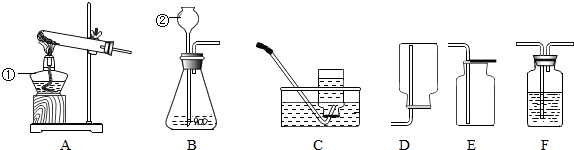
下列实验基本操作正确的是( )
A、给试管里的液体加热时,液体应超过容积的
| ||
| B、稀释浓硫酸时,应将水慢慢注入浓硫酸里 | ||
| C、给试管加热时,应用手拿住试管夹的短柄 | ||
| D、将玻璃导管插入单孔橡皮塞时,应先用水润湿导管口 |
下列说法正确的是( )
| A、NaOH和MgO的混合物中氧的质量分数为40%,NaOH和MgO的质量比为任意值 |
| B、一定量的氯化钠溶液恒温蒸发5克水,析出a克晶体;再蒸发5克水,又析出b克晶体,a与b一定相等 |
| C、用H2完全还原一定质量的CuO,参加反应的H2与通入的H2质量一定相等 |
| D、将98%的浓H2SO4稀释成49%的稀H2SO4,加入水的质量与浓硫酸质量一定相等 |
某学生欲称取4.3g氯化钠,称量过程中发现指针偏右.这时他需要进行的操作是( )
| A、向左移动游码 |
| B、调节平衡螺母 |
| C、增加药品 |
| D、减少药品 |
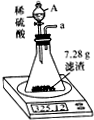
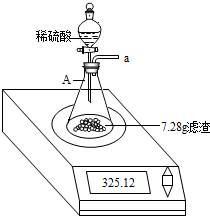 一化学兴趣小组对某月饼包装盒中的“脱氧剂”很好奇,他们观察到“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末.
一化学兴趣小组对某月饼包装盒中的“脱氧剂”很好奇,他们观察到“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末.