题目内容
【题目】2017年5月,我国开采海底可燃冰获得成功。
(1)可燃冰是由甲烷分子和水分子等形成的笼状结构的固体物质,则可燃冰属于___________(填“纯净物”或“混合物”)。
(2)可燃冰中的甲烷完全燃烧的化学方程式为___________。
(3)1 m3可燃冰可释放出约l60-180 m3天然气。从分子性质的角度分析,其主要原因是___________。
(4)图为甲烷转化为其它燃料的微观示意图。下列说法正确的有___________(填标号)。
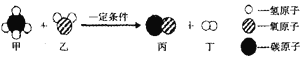
A.以上四种物质都属于化合物
B.反应物乙与生成物丙质量比为9:14
C.反应物甲与生成物丁的分子个数比为1:3
【答案】 混合物 CH4 + 2O2 ![]() CO2 + 2H2O 气体分子间的间隔比固体分子间的间隔大得多 BC
CO2 + 2H2O 气体分子间的间隔比固体分子间的间隔大得多 BC
【解析】本题在可燃冰的情境下考查了物质的分类,化学方程式的书写,微粒的共性,微粒示意图的应用等。
(1)可燃冰是由甲烷分子和水分子等形成的笼状结构的固体物质,是由不同种物质组成的。可燃冰属于混合物;
(2)可燃冰中的甲烷完全燃烧时生成水和二氧化碳,化学方程式为CH4 + 2O2 ![]() CO2 + 2H2O ;
CO2 + 2H2O ;
(3)常温下,可燃冰是固体,甲烷气体。是1 m3可燃冰可释放出约l60-180 m3天然气。从分子性质的角度分析,其主要原因是气体分子间的间隔比固体分子间的间隔大得多。
(4)根据甲烷转化为其它燃料的微观示意图可知该反应的化学方程式为CH4 + H2O![]() CO + 3H2 ;
CO + 3H2 ;
A、以上四种物质中氢气属于单质,不都属于化合物。错误;
B、反应物乙与生成物丙质量比=18:28=9:14,正确;
C、反应物甲与生成物丁的分子个数比为1:3,正确。故选BC。

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案【题目】根据如表回答问题
温度(℃) | 20 | 40 | 50 | 60 | 80 | |
溶解度 (g/100g水) | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |
(1)50℃时,100g水中最多溶解NaCl______ g
(2)A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体。

① A溶液为________(选填“饱和”或“不饱和”)溶液
② 对以下过程的分析,正确的是_________(选填编号)
a.A到B的过程中,溶质质量没有改变 b.B中溶质与溶剂的质量比为169:100
c.A溶液的质量等于222g d.开始析出KNO3固体的温度在60℃至80℃之间