题目内容
【题目】某学习小组对CO2展开研究:

Ⅰ.CO2的制备
(1)写出图中标号仪器的名称:①______。
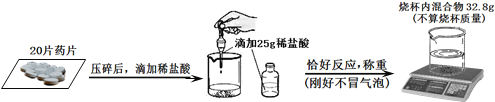
(2)实验室制取CO2的反应原理是为______(写化学方程式)。检查A装置的气密性的一种方法是向分液漏斗中加适量水,堵住右侧导气管,打开分液漏斗活塞,若观察到______,则装置不漏气。
(3)实验发现:制取CO2时,最好选用质量分数为7.5%的稀盐酸。现欲配制100g 7.5%的稀盐酸,需要37%(密度为1.18g / mL)的浓盐酸______mL(计算结果精确到小数点后一位),需要水______mL(精确度同上)。量取水时,若仰视读数(其他操作均正确),则所配稀盐酸的质量分数______7.5%(填“>”或“=”或“<”),配制过程不需要的仪器是______。
A.酒精灯 B.量筒 C.烧杯 D.玻璃棒 E.胶头滴管 F.药匙
Ⅱ.CO2的收集
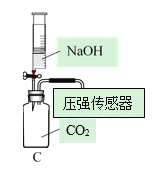
用以下三种方法收集,每种方法均做三次实验,取平均值。将C装置注射器中足量NaOH溶液注入集气瓶中,充分振荡,测集气瓶内气压。(饱和碳酸氢钠溶液可吸收CO2中的HCl气体,NaOH溶液可用来吸收CO2)
方法1:当B装置开始产气泡15s后,用排水法收集 CO2气体,记录集满CO2气体所要的时间为t;
方法2 :当B装置开始产气泡15s后,用向上排空气法收集,收集时间用方法一所用的平均时间t0;
方法3:当B装置开始产气泡15s后,用向上排空气法收集,同时用燃着木条放在集气瓶口,待木条熄灭,立即盖上玻璃片。
实验数据:
方法1 | 方法2 | 方法3 | |
瓶内初始气压(kPa) | 104.2 | 104.2 | 104.2 |
三次实验最终气压平均值(kPa) | 9.3 | 31.8 | 39.7 |
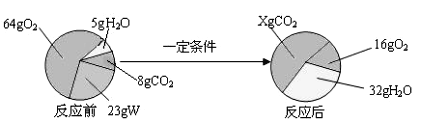
CO2纯度 | 91.1% | 69.5% | X |
数据
(4)三种方法均在15s后开始收集的原因是______。
(5)已知:CO2纯度 =![]() ,则方法3所收集CO2的纯度为______。通过对比,欲收集更高纯度的CO2,应采用______法收集。
,则方法3所收集CO2的纯度为______。通过对比,欲收集更高纯度的CO2,应采用______法收集。
Ⅲ.二氧化碳转化新进展
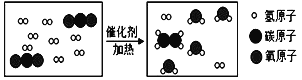
(6)利用非高热电浆体合成技术可将CO2和甲烷(CH4)反应合成乙酸(CH3COOH),反应的化学方程式为______。
(7)在光催化条件下,CO2和H2反应生成甲烷(CH4)和水,反应的化学方程式为______。
【答案】锥形瓶 CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ 分液漏斗末端出现稳定的水柱 17.2mL 79.7 mL < AF 为了排净装置内的空气 61.9% 排水法 CO2+ CH4=CH3COOH CO2+4H2![]() CH4+ 2H2O
CH4+ 2H2O
【解析】
(1)仪器①的名称为:锥形瓶。
(2)实验室用大理石和稀盐酸反应制取CO2,反应方程式为CaCO3 + 2HCl == CaCl2 + H2O + CO2↑。检查A装置的气密性的一种方法是向分液漏斗中加适量水,堵住右侧导气管,打开分液漏斗活塞,若观察到分液漏斗末端出现稳定的水柱,则装置不漏气。
(3)设配制100g 7.5%的稀盐酸,需要37%(密度为1.18g/mL)的浓盐酸体积为V,则:37%×1.18g/mL×V=100g×7.5% ,解得V≈17.2mL;需要水的质量为:100g-17.2mL×1.18g/mL=79.7g,水的体积为:79.7g÷1g/mL=79.7mL;量取水时,若仰视读数(其他操作均正确),造成量取的水偏多,则所配稀盐酸的质量分数偏小;配制过程不需要A、酒精灯和F、药匙。
(4)三种方法均在15s后开始收集的原因是为了排净装置内的空气;
(5)方法3所收集CO2的纯度为:CO2纯度 =![]() =(1-
=(1-![]() )×100%=61.9%。通过对比,欲收集更高纯度的CO2,应采用排水法收集。
)×100%=61.9%。通过对比,欲收集更高纯度的CO2,应采用排水法收集。
(6)利用非高热电浆体合成技术可将CO2和甲烷(CH4)反应合成乙酸(CH3COOH),反应的化学方程式为:CO2+ CH4=CH3COOH;
(7)在光催化条件下,CO2和H2反应生成甲烷(CH4)和水,反应的化学方程式为:CO2+4H2![]() CH4+ 2H2O。
CH4+ 2H2O。

 名校课堂系列答案
名校课堂系列答案【题目】控制变量法是实验探究的重要方法。下列四组对比实验获得的结论不正确的是
序号 | 实验操作 | 结论 |
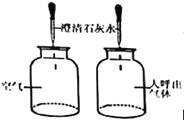
A |
| 呼出的气体全部都是CO2 |
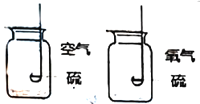
B. |
| O2含量越高,反应越剧烈 |
C. |
| 燃烧需要温度达到可燃物的着火点 |
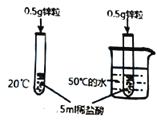
D |
| 温度越高,化学反应速率越快 |
A. A B. B C. C D. D
【题目】某实验小组用氯酸钾和二氧化锰混合加热制取氧气时,发现制得的气体有刺激性气味,于是对该气体成分进行探究
(提出问题)氯酸钾与氧化锰混合加热后产生的气体成分是什么?
(查阅资料)
(1)氯酸钾与二氧化锰混合加热产生的气体只以单质形式存在;
(2)氯气(C12)的性质:
①有剌激性气味的气体;②溶于水;③能使湿润的淀粉碘化钾试纸变蓝。
(猜想与假设)
猜想一:该气体为O2;猜想二,该气体为Cl2;猜想三:该气体为________________________。
(实验探究)
序号 | 实验操作 | 实验现象 | 实验结论 |
1 | 小丽用排水集气法收集A、B两瓶气体,将带火星木条伸入A中,湿的淀粉碘化钾试纸伸入B中 | A中带火星木条复燃,B中淀粉碘化钾试纸不变色 | 猜想____________成立 |
2 | 小岚向上排空气法收集C、D两瓶气体,将带火星木条伸入C中,湿润的淀粉碘化钾试纸伸入D中 | C中带火星木条复燃,D中淀粉碘化钾试纸______。 | 猜想三成立 |
(反思与评价)
小涛认为小丽的结论不正确,原因是_____________________。
(拓展应用)
实验室通常用MnO2与浓盐酸共热制取Cl2,请完成该反应的化学方程式MnO2+4HCl(浓)![]() MnCl2 +____________ +Cl2↑
MnCl2 +____________ +Cl2↑