题目内容
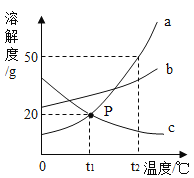
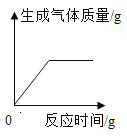
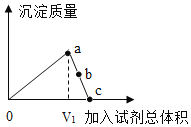
【题目】向一定质量的CuSO4溶液中滴加KOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列有关说法不正确的是
A.加入试剂总体积为V1时,溶液中不存在KOH
B.b点时所加试剂一定是稀盐酸
C.c点时溶液中的溶质都是盐
D.a点时溶液中一定不存在Cu2+
【答案】D
【解析】
氢氧化钾与硫酸铜反应生成氢氧化铜和硫酸钾,氢氧化铜与盐酸反应生成氯化铜和水。
A、加入试剂总体积为V1时,沉淀质量达到了最大值,滴加稀盐酸后沉淀的质量立即开始减少,此时溶液中不存在KOH,故A正确;
B、a点后,沉淀质量逐渐减少,所以b点时所加试剂一定是稀盐酸,故B正确;
C、c点时,盐酸和氢氧化铜恰好完全反应,所以溶液中的溶质都是盐,故C正确;
D、向一定质量的CuSO4溶液中滴加KOH溶液一段时间后,滴加稀盐酸后沉淀的质量立即开始减少,由于硫酸铜不与稀盐酸反应,可能是硫酸铜有剩余,无法确定a点时溶液中是否存在Cu2+,溶液可能存在Cu2+,故D错误。故选D。

 阅读快车系列答案
阅读快车系列答案【题目】酸、碱、盐是初中化学学习的重要知识。根据所学知识,某化学兴趣小组设计了如下两个实验,探究氢氧化钠与二氧化碳的反应。
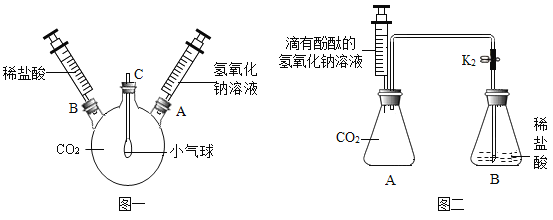
(1)如图一装置所示,先将氢氧化钠溶液注入三颈烧瓶中,然后再将稀盐酸注入三颈烧瓶中,观察到气球的变化是________________,产生这一现象的原因是_______________。
(2)根据实验一的原理,兴趣小组的同学又设计了图二装置。实验前关闭K,先将注射器中的氢氧化钠溶液注入A中,然后再打开K,稀盐酸倒流进A中,片刻后停止倒流,A中溶液仍为红色。同学们对反应后A装置中的溶液成分产生了兴趣,提出了如下猜想:
猜想一: NaCl、 Na2CO3
猜想二: NaCl、 NaOH
猜想三: NaCl、NaOH、Na2CO3
①上述猜想不合理的是___________,原因是______。
同学们经过讨论设计了如下实验方案进行探究
实验操作 | 实验现象 | 实验结论或化学方程式 |
②__________________ | 有白色沉淀产生 | ③反应的化学方程式__________ |
静置,取上层清液,向其中滴加酚酞溶液 | ④_________________ | 猜想三成立 |
(3)上述实验结束后,兴趣小组的同学想将溶液的溶质都变为NaCl。他们向装置A中加入20g溶质质量分数为7.3%稀盐酸,恰好使红色完全退去,试计算反应后NaCl的质量增加了_______?