题目内容
【题目】(2011年浙江宁波,19题、)将一定量的苯(C6H6)和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水和一种未知物X。测得反应前后物质的质量如下表:
物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
下列判断正确的是 ( )
A.表中m的值为13.5 B.该反应属于分解反应
C.物质X能在氧气中燃烧 D.物质X中一定含有氢元素
【答案】C
【解析】
根据质量守恒定律,苯、氧气质量都减少,为反应物,而二氧化碳和水的质量增加为生成物,M苯+M氧气=3.9g+9.6g=13.5g,M二氧化碳+M水="6.6g+2.7g=9.3" g,13.5g >9.3 g,故X反应的质量为m="13.5" g -11.6 g=1.9g,故A、B说法错误;3.9g苯含氢元素质量=3.9g×6/78="0.3g" ,7.2g水含氢元素的质量为2.7g×2/18=0.3g,二者含氢元素质量相等,说明X不可能含有氢元素,D说法错误;2.7g水含氧元素的质量为2.7g×16/18=2.4g, 6.6g二氧化碳含氧元素的质量为6.6g×32/44=4.8g,二者之和2.4g+4.8g=7.2g,故X含有氧元素质量为9.6g-7.2g=2.4g,3.9g苯含碳元素3.9g×72/78=3.6g,6.6g二氧化碳含碳元素的质量为6.6g×12/44=1.8g。则X含碳元素的质量为3.6g-1.8g=1.8g;则X中碳元素与氧元素所含有原子个数为![]() :
:![]() =1:1,故X的化学式为CO,CO能在氧气中燃烧,C说法正确。答案为C。
=1:1,故X的化学式为CO,CO能在氧气中燃烧,C说法正确。答案为C。

 新课标阶梯阅读训练系列答案
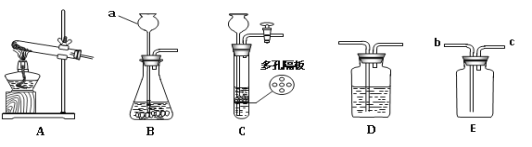
新课标阶梯阅读训练系列答案【题目】某兴趣小组同学利用下图所示装置进行“铝与硫酸铜溶液反应”的实验时,发现反应开始后试管中出现红色固体同时产生无色无味气体。兴趣小组同学进行了以下探究。

实验1:向5份相同体积的硫酸铜溶液中分别加入表面经过打磨处理的相同长度的铝条,现象如下:
实验组别 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
硫酸铜溶液浓度 | 24% | 12% | 8% | 6% | 5% | 3% | 1% |
气泡情况 | 很快 | 快 | 较快 | 快 | 较快 | 慢 | 无 |
实验2:向质量分数为8%的硫酸铜溶液分别加入表面经过打磨处理的相同长度的铝条,现象如下:
实验组别 | ① | ② | ③ | ④ | ⑤ |
水浴温度(℃) | 20 | 30 | 40 | 50 | 60 |
气泡情况 | 较快 | 快 | 很快 | 很快 | 很快 |
(1)实验1的目的是______。
(2)实验2的结论是______。
(3)依据实验1和实验2,推测50℃ 5% 硫酸铜溶液与铝条反应的现象是________。
(反思与评价)
(4)实验2没有进行温度为70℃的实验,理由是_______。
(5)根据你的猜想,气泡中的气体是______。
【题目】(3分)有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应)。课外小组为了测定该石灰石样品中碳酸钙的质量分数,将一定量的石灰石样品放入烧杯中,再取100 g稀盐酸分4次加入烧杯中,每次均充分反应。实验数据记录如下:
次数 | 第1次 | 第2次 | 第3次 | 第4次 |
加入稀盐酸质量 /g | 25 | 25 | 25 | 25 |
反应后烧杯中物质的总质量 /g | 35.2 | 58.4 | 82.6 | 107.6 |
求:(1)第1次加入稀盐酸充分反应后,生成二氧化碳的质量是 g。
(2)该石灰石样品中碳酸钙的质量分数。