题目内容
某化学实验活动小组的同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。参与他们进行的探究活动:
【提出问题】久置氢氧化钠固体的成分是什么?
【猜想与假设】
猜想Ⅰ:全部是NaOH;
猜想Ⅱ:全部是Na2CO3; 猜想Ⅲ: 。
【实验与探究】
(1)分析:暴露在空气中的氢氧化钠会变质,变质原因是(用化学方程式表示)______________________
(2)实验如下:
(3)为了进一步的验证猜想结果,小明同学提出如下实验方案:继续步骤二的实验,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想_________成立;若酚酞不变红,则猜想______成立。
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈 性(填“酸”或“碱”),能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是 。
【提出问题】久置氢氧化钠固体的成分是什么?
【猜想与假设】
猜想Ⅰ:全部是NaOH;
猜想Ⅱ:全部是Na2CO3; 猜想Ⅲ: 。
【实验与探究】
(1)分析:暴露在空气中的氢氧化钠会变质,变质原因是(用化学方程式表示)______________________
(2)实验如下:
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 步骤一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的_________。 | 实验过程中始终没有气泡产生。 | 则证明猜想 成立。 |
| 步骤二:另取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氯化钡溶液。 | 实验过程中产生 | 则证明猜想Ⅱ或Ⅲ成立。此过程中发生反应的化学方程式为 _____________________ |
(3)为了进一步的验证猜想结果,小明同学提出如下实验方案:继续步骤二的实验,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想_________成立;若酚酞不变红,则猜想______成立。
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈 性(填“酸”或“碱”),能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是 。
NaOH和Na2CO3的混合物
(1)2NaOH + CO2 = Na2CO3 + H2O
(2)稀盐酸 Ⅰ 白色沉淀 Na2CO3+BaCl2=BaCO3↓+2NaCl
(3)Ⅲ Ⅱ 碱 滴加过量氯化钡溶液
(1)2NaOH + CO2 = Na2CO3 + H2O
(2)稀盐酸 Ⅰ 白色沉淀 Na2CO3+BaCl2=BaCO3↓+2NaCl
(3)Ⅲ Ⅱ 碱 滴加过量氯化钡溶液
试题分析:【猜想与假设】可能是部分变质,所以猜想:NaOH和Na2CO3的混合物
(1)暴露在空气中的氢氧化钠会变质,是由于吸收了空气中的二氧化碳,发生反应:2NaOH + CO2 = Na2CO3 + H2O
(2)抓住碳酸钠与氢氧化钠的性质不同、碳酸钠会与盐酸反应产生气体,所以要验证有没有碳酸钠,应滴加足量的盐酸,因为实验过程中始终没有气泡产生。说明没有碳酸钠,则证明猜想Ⅰ成立,步骤二,滴加氯化钡溶液,若有碳酸钠,则发生反应:Na2CO3+BaCl2=BaCO3↓+2NaCl,现象是有白色沉淀生成
(3)步骤二只证明了含有碳酸钠,但是不是含有氢氧化钠并不清楚,所以为了进一步的验证猜想结果,小明同学提出如下实验方案:继续步骤二的实验,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,说明里面还含有氢氧化钠,证明则猜想Ⅲ成立,若酚酞不变红,说明里面不含有氢氧化钠,则猜想Ⅱ成立。因为碳酸钠溶液也呈碱性,,所以在证明氢氧化钠存在的时候,必须保证没有碳酸钠的干扰,所以该方案的操作步骤中应该改进的是:滴加过量氯化钡溶液,以除去溶液中的碳酸钠

练习册系列答案
相关题目
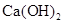 溶液、Na2CO3溶液中的一种。请你将它们区分出来,并完成下面的实验报告。
溶液、Na2CO3溶液中的一种。请你将它们区分出来,并完成下面的实验报告。