题目内容
【题目】如图所示四个图像,分别对应四个过程,其中不正确的是
A.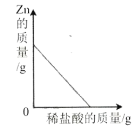 向一定量的锌中加入足量的稀盐酸
向一定量的锌中加入足量的稀盐酸
B.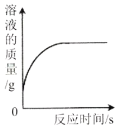 向一定量硫酸铜溶液中加入足量的铁
向一定量硫酸铜溶液中加入足量的铁
C.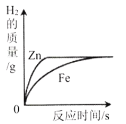 足量锌、铁中分别加入等质量、等质量分数的稀硫酸
足量锌、铁中分别加入等质量、等质量分数的稀硫酸
D.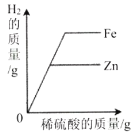 等质量的锌和铁中分别加入足量等质量分数的稀硫酸
等质量的锌和铁中分别加入足量等质量分数的稀硫酸
【答案】B
【解析】
A、向一定量的锌中加入足量的稀盐酸,锌完全反应后质量为0,不符合题意;
B、向一定量硫酸铜溶液中加入足量的铁,铁和硫酸铜反应生成硫酸亚铁和铜,![]() ,每56g固体铁加入置换出64g铜单质,反应后固体质量增加,溶液的质量减小,反应完后不再减小,符合题意;
,每56g固体铁加入置换出64g铜单质,反应后固体质量增加,溶液的质量减小,反应完后不再减小,符合题意;
C、足量锌、铁中分别加入等质量、等质量分数的稀硫酸,锌的活动性强,在相同的时间内生成的氢气多,稀硫酸的质量相同,完全反应后生成的氢气相同,不符合题意;
D、等质量的锌和铁中分别加入足量等质量分数的稀硫酸,相同的酸反应,生成的氢气质量相同,根据反应方程式:![]()
![]() 每生成2g氢气需要锌的质量为65g,需要铁的质量为56g,等质量的锌和铁中分别加入足量等质量分数的稀硫酸,完全反应后,铁生成的氢气多,不符合题意。故选B。
每生成2g氢气需要锌的质量为65g,需要铁的质量为56g,等质量的锌和铁中分别加入足量等质量分数的稀硫酸,完全反应后,铁生成的氢气多,不符合题意。故选B。

 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案【题目】同学们在实验室举行创新实验活动时,对防毒面具罐体內物质产生了浓厚的兴趣并对其展开了探究。
(查阅资料)防毒面具里通常有滤毒罐和生氧罐。①滤毒罐中的活性炭能滤去有毒气体,这是利用活性炭的______性。②生氧罐中装有过氧化钠生氧剂,在通常情况下,过氧化钠是一种粉末状固体,过氧化钠与水和二氧化碳都能反应,其化学方程式为![]() ,
,![]() 。
。
(提出问题)使用一段时间后,生氧罐内的固体粉末是什么?
(猜想与假设)猜想一:Na2CO3
猜想二:Na2CO3和Na2O2
猜想三:Na2CO3和NaOH
猜想四:Na 2CO3、 Na2O2和NaOH
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
①取少量样品于试管中,加入足量的水,振荡 | ____ | 不含Na2O2 |
②在步骤①所得的溶液中滴加____,振荡 | 产生白色沉淀 | 含Na2CO3 |
③在步骤②所得的溶液中滴加_____,振荡 | 溶液变红 | 含__ |
(得出结论)猜想____正确。
(交流与反思)(1)请写出步骤②中发生反应的化学方程式:_______。
(2)小红认为将步骤②③所用试剂调换也可以得出正确的结论,理由是______。
【题目】食品工业中碘化钾(KI)可用作营养增补剂。碘化钾是白色固体,在空气中久置会“泛黄”变质。某实验小组对碘化钾变质后的成分及变质的条件进行探究。
I.探究变质后的固体成分
(查阅资料)淀粉溶液遇碘(I2)变蓝。
(进行实验)
实验 1
编号 | ① | ② |
操作及现象 | 加热变质后的 KI 固体,黄色消失, 产生的紫色蒸气使淀粉溶液变蓝。 | 向变质后的 KI 固体中滴加稀盐酸, 产生的气体使澄清石灰水变浑浊。 |
II.探究变质的条件
(猜想与假设)常温下,KI 固体“泛黄”变质可能与 O2、CO2 和水蒸气有关。
(进行实验)
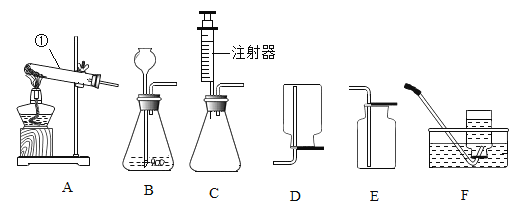
实验 2:利用下图装置和表中所列物质分别进行实验,放置相同时间,现象如下表。
装置 | 编号 | ① | ② | ③ | ④ |
| 试管中的物质 | O2 和 H2O | O2 和 CO2 | H2O 和 CO2 | O2、CO2 和H2O |
固体颜色 | 无明显变化 | 无明显变化 | 无明显变化 | 固体泛黄 |
(解释与结论)
(1)实验 1 中石灰水变浑浊的原因是_________(用化学方程式表示)。
(2)由实验 1 中现象推知,“泛黄”变质后的固体中含有的物质是________。
(3)由实验 2 得出“KI 变质一定与 O2 有关”的结论,依据的两个实验是________(填编号)。
(4)由实验 2 推知,KI“泛黄”变质的条件是_________。
III.依据初步结论,深入探究变质的条件
实验 3:分别取相同浓度的 KI 溶液进行实验,在空气中放置相同时间,现象如下表。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
溶液颜色 | 无色 | 浅黄色 | |||
(5)实验 3 中,观察到③~⑤溶液颜色依次加深,推测其原因是________。
(6)由实验 3 推知,KI 固体久置“泛黄”变质过程中,CO2 起到的作用是________。