题目内容
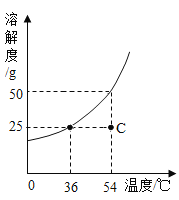
【题目】t℃时,120g某硝酸钾溶液蒸发去17.5g水析出2.5g硝酸钾,若原溶液蒸发去27.5g水并恢复到t℃,则析出5g硝酸钾晶体,由此判断下列说法正确的是
A.原溶液浓度为20%B.蒸发后溶液浓度为25%
C.t℃时硝酸钾溶解度为25gD.原溶液中硝酸钾的质量为20g
【答案】C
【解析】
t℃时,120g某硝酸钾溶液蒸发去17.5g水析出2.5g硝酸钾,若原溶液蒸发去27.5g水并恢复到t℃,则析出5g硝酸钾晶体,则饱和溶液中每10g水中含有2.5g硝酸钾;饱和溶液质量分数为![]()
A、原溶液浓度为x,![]() ,x=18.75%;故选项错误。
,x=18.75%;故选项错误。
B、蒸发后溶液变为饱和溶液,浓度为![]() ;故选项错误。
;故选项错误。
C、t℃时,饱和溶液中每10g水中含有2.5g硝酸钾,则硝酸钾的溶解度为25g;故选项正确。
D、原溶液中硝酸钾的质量为:120g![]() 18.75%=22.5g;故选项错误。
18.75%=22.5g;故选项错误。
故选:C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目